Viiib-группа
Cтраница 3
Уменьшение гат в ряду d - элементов называется d - сжатием. Сжатие особенно заметно у атомов элементов VIIIB-группы. Уменьшение гат с ростом порядкового номера в ряду лантаноидов называется лантаноидным сжатием. Оно происходит в результате усиления притяжения электронов к ядру с ростом заряда ядра. [31]
В четвертый период входят ( в порядке заполнения электронами d - орбиталей третьего уровня атомов) скандий Sc, титан Ti, ванадий V, хром Сг, марганец Мп, занимающие места соответственно с IIIB - по VIIB-группу. Железо Fe, кобальт Со и никель Ni находятся в VIIIB-группе, образуя ее первую триаду - семейство железа. Медь Си и цинк Zn располагаются соответственно в IB - и ПВ-группе. [32]
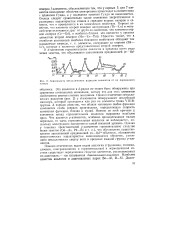 |
Зависимость металлических радиусов элементов от их порядкового номера. [33] |
Эта аналогия в d - рядах не может быть обнаружена при сравнении потенциалов ионизации, потому что для этих элементов свойственны разные степени окисления. Однако изменение металлических радиусов ( рис. 2) у с ( - элементов обнаруживает неглубокий минимум, который приходится как раз на элементы триад VIIIB-группы. Именно по этой причине у элементов триад горизонтальная аналогия выражена наиболее ярко. Что касается р-элементов, особенно принадлежащих малым периодам, то здесь горизонтальная аналогия не наблюдается, поскольку электронами заполняется самый внешний уровень. [34]
У элементов VIIIB-группы ковалентность, равная номеру труппы, проявляется лишь у рутения Ru и у осмия Os. У железа Fe высшая ковалентность шесть, а типичны для него двух - и трехковалентности. Элементы VIIIB-группы ( иначе VIII, IX и ХВ-групп) не проявляют, как правило, ковалентность, равную номеру группы, потому что у них часть ( п - 1) й-электронов спарена. [35]
Элементы триады железа имеют валентную электронную конфигурацию 3de4s2, 3d 4s2, 3d4s2 для Fe, Co, Ni соответственно. Следовательно, в VIIIB-группе наблюдается уникальное в периодической системе явление: число валентных электронов элемента ( Со, Ni) превосходит номер группы. [36]
Железо, кобальт и никапъ образуют непрерывные твердые растворы не только между собой, но и с другими переходными металлами. Так, о железо образует неограниченные твердые растворы с V и Сг ( ОЦК), - / - железо и / - кобальт ( ГЦК) с - / - марганцем ( ГЦК), родием, иридием, палладием и платиной. Последнее подтверждает определенную аналогию между всеми элементами VIIIB-группы. Кобальт ( ГПУ) непрерывно взаимно растворим с изоморфными Re, Ru, Os. Никель обнаруживает металлохимическое сходство с j - Fe и / 3 - Со, но в отличие от них образует непрерывные твердые растворы с металлами IB-группы - медью и золотом. Таким образом, элементы VIIIB-группы служат своеобразным связующим звеном между металлами VIIB - и IB-групп. [37]
Железо, кобальт и никель образуют непрерывные гвердые растворы не только между собой, но и с другими переходными металлами. Так, о - железо образует неограниченные твердые растворы с V и Сг ( ОЦК), 7-железо и / Исобатт ( ГЦК) с 7-марганцем ( ГЦК), родием, иридием, палладием и платиной. Последнее подтверждает определенную аналогию между всеми элементами VIIIB-группы. Кобальт ( ГПУ) непрерывно взаимно растворим с изоморфными Re, Ru, Os. Никель обнаруживает металлохимическое сходство с 7 - Fe и / 3 - Со, но в отличие от них образует непрерывные твердые растворы с металлами IB-группы - медью и золотом. Таким образом, элементы VIIIB-группы служат своеобразным связующим звеном между металлами VIIB - и IB-групп. [38]
Непрерывные твердые растворы - y - U образует с Np, Pu, Ti, Zr, Nb. При ограниченной взаимной растворимости уран образует значительное число интерметаллических соединений, особенно с элементами VIIIB-группы. [39]
 |
Зависимость металлических радиусов элементов от их порядкового номера. [40] |
Для / - элементов горизонтальная аналогия в пределах всего ряда менее заметна, что обусловлено заполнением предвнешней ( и - 1) йболочки. Эта аналогия в rf - рядах не может быть обнаружена при сравнении потенциалов ионизации, потому что для этих элементов свойственны разные степени окисления. Однако изменение металлических радиусов ( рис. 119) у d - элементов обнаруживает неглубокий минимум, который приходится как раз на элементы триад VIIIB-группы. Именно по этой причине у элементов триад горизонтальная аналогия выражена наиболее ярко. Что касается р-элементов, особенно принадлежащих малым периодам, то здесь горизонтальная аналогия не наблюдается, поскольку электронами заполняется самый внешний уровень. [41]
 |
Зависимость металлических радиусов элементов от их порядкового номера. [42] |
Для rf - элементов горизонтальная аналогия в пределах всего ряда менее заметна, что обусловлено заполнением предвнешней ( п - 1) / - оболочки. Эта аналогия в d - рядах не может быть обнаружена при сравнении потенциалов ионизации, потому что для этих элементов свойственны разные степени окисления. Однако изменение металлических радиусов ( рис. 119) у d - элементов обнаруживает неглубокий минимум, который приходится как раз на элементы триад VIIIB-группы. Именно по этой причине у элементов триад горизонтальная аналогия выражена наиболее ярко. Что касается р-элементов, особенно принадлежащих малым периодам, то здесь горизонтальная аналогия не наблюдается, поскольку электронами заполняется самый внешний уровень. Однако у тяжелых представителей р-эле-ментов горизонтальное сходство более заметно ( Ge - As, Pb - Bi и т.п.), что обусловлено существованием предвнешней заполненной ( п - 1) ( Р - оболочкй, сближением энергетических характеристик заполняющихся оболочек, усилением металличности сверху вниз в пределах каждой группы р-элементов. [43]
Наибольшее количество промежуточных фаз типа соединений Курнакова образуется при взаимодействии элементов подгруппы хрома с триадой железа и платиновыми металлами ( CrFe, CrNi, CrCo. При этом состав соединений Курнакова никогда не обогащен элементом VIB-группы. Поскольку соединения Курнакова образуются из твердых растворов ( непрерывных или ограниченных), можно сделать вывод, что элементы VIB-группы значительно лучше растворимы в металлах VIIIB-группы, чем последние в хроме и его аналогах. [44]
В целом VIII группа состоит из инертных ( Не, Ne) и благородных газов ( Ar, Kr, Xe, Rn), объединяемых в VIIIA-группу, и металлов VIIIB-группы. VIIIB-группа также резко отличается в структурном отношении от остальных групп периодической системы. Однако триада железа заметно отличается по свойствам от двух остальных триад в силу кайносимметричности Sd-оболочки. Поэтому при рассмотрении свойств элементов VIIIB-группы выделяют элементы семейства железа и платиновые металлы, включающие остальные элементы. Кроме того, семейство платиновых металлов целесообразно подразделить на три вертикальные диады ( Ru-Os, Rh-Ir, Pd-Pt), в пределах которых свойства элементов особенно близки, что обусловлено лантаноидной контракцией. [45]
Страницы: 1 2 3 4