Ионный проводник
Cтраница 2
 |
Электрохимические ячейки с различными электродами по Вагнеру [ 3J. [16] |
В этом примере ионный проводник AgCl обусловливает чисто ионную проводимость и вследствие этого появление потенциала только относительно иона серебра. [17]
В дальнейшем рассматриваются преимущественно ионные проводники - растворы электролитов, и лишь бегло - некоторые другие группы проводников. [18]
В дальнейшем рассматриваются преимущественно ионные проводники - растворы электролитов, и лишь бегло - некоторые другие группы проводников. [19]
В отличие от ионных проводников, для которых, как отмечалось в предыдущем разделе, выбор носителей бывает двояким, для электронных проводников носители принято выбирать вполне однозначно: это электроны в зоне проводимости для проводников - типа и электронные дырки для проводников р-типа. Поэтому для них подвижность всегда относится к указанным частицам. [20]
Существуют различные классы ионных проводников. [21]
Температурный коэффициент электропроводности ионных проводников положителен. [22]
 |
Водородный электрод правлению, движения электронов1. Следовательно, ток. [23] |
Такой мостик служит ионным проводником между двумя сосудами, чтобы не допустить непосредственного смешения растворов сульфата цинка и сульфата меди. [24]
Поскольку Agl является ионным проводником, не проводящим электроны, то поглощение электронов будет происходить вблизи границы Ag2S - Agl точно так же, как и выделение серебра в предыдущем случае. Это приводит к возникновению градиента концентрации электронов, направленного слева направо. [25]
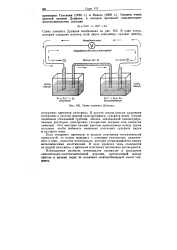 |
Схема элемента Даниэля. [26] |
Этот мостик служит ионным проводником между двумя сосудами, чтобы избежать смешения растворов сульфата цинка и сульфата меди. [27]
Электролиты ХИТ служат ионными проводниками тока ( проводниками 2-го рода) между электродами, а также отделяют восстановитель от непосредственного контакта с окислителем. К электролитам ХИТ предъявляются следующие основные требования: 1) высокая ионная электрическая проводимость; 2) очень низкая электронная проводимость; 3) малая коррозионная активность ( лучше инертность) к электродам и конструкционным материалам элементов; 4) устойчивость при работе элемента и его хранении, а также при контакте с восстановителем, окислителем и продуктами реакции. [28]
Твердый LiH такой же хороший ионный проводник, как LiCl, и в 1000 раз лучший, чем LiF. При электролизе расплава LiH со стальными электродами при температуре лишь немного выше температуры плавления на катоде выделяется литий, а на аноде - водород. Эти ионные гидриды имеют значительно более высокие температуры плавления, чем рассмотренные выше молекулярные гидриды, например LiH 691 С, NaH 700 - 800 С ( с разложением); гидриды других щелочных металлов разлагаются до плавления. Все они энергично реагируют с водой, выделяя водород и давая раствор гидроксида. [29]
Экспериментальное изучение чисел переноса ионных проводников встретило ряд трудностей, которые серьезно ограничили возможности этого метода. [30]
Страницы: 1 2 3 4