Продолжение - хлорирование
Cтраница 1
Продолжение хлорирования в стеклянном сосуде на ярком солнечном свету ведет непосредственно к CC13CF2CF2CC13, однако процесс идет очень медленно. [1]
 |
Условия и состав продуктов хлорирования 2-хлор - и 2 5-дихлор-п - ксилолов. [2] |
Продолжение хлорирования приводит к отщеплению хлорметильной группы и образованию соответствующих хлорбензо-лов. [3]
Для продолжения хлорирования температуру поднимают на 10 - 20 град и снова пропускают хлор до ослабления выделения хлористого водорода. [4]
 |
Содержание активного хлора в различных хлорсодержащих продуктах. [5] |
После поглощения хлора в количестве, отвечающем продукту III, выпадают его кристаллы, которые при продолжении хлорирования постепенно переходят в раствор. В щелоке должно содержаться примерно 0 5 % Са ( ОН) 2, чтобы не образовывалась свободная хлорноватистая кислота, которая будет окислять продукт до хлората. [6]
Затем прибавляют 0 2 г амальгамированного алюминия и продолжают пропускать хлор, пока привес де составит 4 6 г. В продолжение хлорирования колбу охлаждают. Продукт реакции состоит в основном из смеси о - и р-дихлор-бензолов. Промыванием водой и растворо-м едкого натра удаляют избыток хлора и хлористый водород. После этого продукт высушивают и охлаждают в охладительной смеси, причем выкристаллизовывается большая часть р-дихлорбензола, который отделяют. Для разделения о - от р-изомера пользуются стойкостью р-дихлорбензола к сульфированию. К жидкости прибавляют равный объем дымящей - серной кислоты и через час к смеси осторожно прибавляют лед. Продукт сульфирования подвергают перегонке с водяным паром, причем в перегонной колбе укрепляют термометр, шарик которого погружен в жидкость. [7]
Затем прибавляют 0 2 г амальгамированного алюминия и продолжают пропускать хлор, пока привес де составит 4 6 г. В продолжение хлорирования колбу охлаждают. Продукт реакции состоит в основном из смеси о - и р-дихлор-бензолов. Промыванием водой и растворо-м едкого натра удаляют избыток хлора и хлористый водород. После этого продукт высушивают и охлаждают в охладительной смеси, причем выкристаллизовывается большая часть р-дихлорбензола, который отделяют. Для разделения о - от р-изомера пользуются стойкостью р-дихлорбензола к сульфированию. К жидкости прибавляют равный объем дымящей верной кислоты и через час к смеси осторожно прибавляют лед. Продукт сульфирования подвергают перегонке с водяным паром, причем в перегонной колбе укрепляют термометр, шарик которого погружен в жидкость. [8]
Затем прибавляют 0 2 г амальгамированного алюминия и продолжают пропускать хлор, пока ( привес де составит 4 6 г. В продолжение хлорирования колбу охлаждают. Продукт реакции состоит в основном из смеси о - и р-дихлор-бензолов. Промыванием водой и растворо-м едкого натра удаляют избыток хлора и хлористый so - дород. После этого продукт высушивают и охлаждают в охладительной смеси, причем выкристаллизовывается большая часть р-ди-хлорбензола, который отделяют. Фильтрат состоит главным образом из о-дихлорбенаола и содержит в растворе некоторое количество р-щомера и трихлорбензола. Для разделения о - от р-изомера пользуются стойкостью р-дихло рбензола к сульфированию. К жидкости прибавляют равный объем дымящей - серной кислоты и через час к смеси осторожно прибавляют лед. Продукт сульфирования подвергают перего Нке с водяным паром, причем в перегонной колбе укрепляют термометр, шарик которого погружен в жидкость. [9]
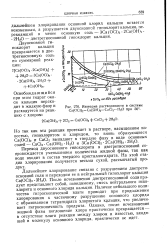 |
Изотерма растворимости в системе Са ( ОС1 2 - Са ( ОН2 - СаС12 - Н2О при 50. [10] |
После исчезновения дветретиосновной соли продукт представляет собой, повидимому, смесь нейтрального гипохлорита и основного хлорида кальция. Наличие небольшого количества гигроскопической влаги приводит при продолжении хлорирования к частичному разрушению основного хлорида с образованием тетрагидрата хлористого кальция, что увеличивает гигроскопичность продукта. Однако, после исчезновения жидкой фазы поглощение хлора практически прекращается - в отсутствие влаги реакция между хлором и известью, входящей в молекулу основного хлорида, практически не идет. [11]
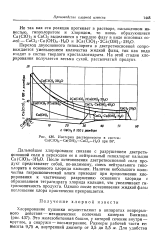 |
Изотерма растворимости в система Са ( С1О 2 - Са ( ОН2 - СаС12 - Н2О при 50. [12] |
После исчезновения дветретиосновной соли продукт представляет собой, по-видимому, смесь нейтрального гипо-хлорита и основного хлорида кальция. Наличие небольшого количества гигроскопической влаги приводит при продолжении хлорирования к частичному разрушению основного хлорида с образованием тетрагидрата хлорида кальция, что увеличивает гигроскопичность продукта. Однако после исчезновения жидкой фазы поглощение хлора практически прекращается. [13]
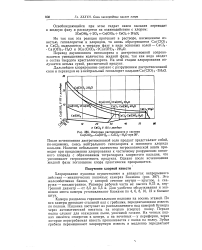 |
Изотерма растворимости в системе Са ( СЮ2 - Са ( ОН2 - СаС12 - Н2О при 50. [14] |
После исчезновения дветретиосновной соли продукт представляет собой, по-видимому, смесь нейтрального гипохлорита и основного хлорида кальция. Наличие небольшого количества гигроскопической влаги приводит при продолжении хлорирования к частичному разрушению основного хлорида с образованием тетрагидрата хлористого кальция, что увеличивает гигроскопичность продукта. Однако после исчезновения жидкой фазы поглощение хлора практически прекращается. [15]
Страницы: 1