Продукт - первая реакция
Cтраница 1
Продукт первой реакции называется фосфином, а второй - силаном. [1]
Строение N-алкилированных продуктов первой реакции было доказано при помощи некоторых физических методов, а также по реакциям гидролитического расщепления. [2]
Ими был выделен продукт первой реакции, а именно тиодифторфосфорная кислота H ( OPSF2) в виде хорошо кристаллизующейся нитронной соли с выходом 75 % от теории. [3]
Для отделения бора от продуктов первой реакции полученную смесь нагревают с разбавленной хлороводородной кислотой, переводящей в раствор В2Оз в виде В ( ОН) з, a Mg и MgO в виде MgCb. Бор отфильтровывают и подвергают дальнейшей очистке. Продукты второй реакции обрабатывают при нагревании водой, растворяющей все реагенты, кроме бора. [4]
Сопряженные реакции применяются в аналитических методиках [13] либо для превращения продуктов первой реакции в более легко измеряемую форму, либо для обеспечения энергией, чтобы сместить первую реакцию в направлении, которое может быть неблагоприятным с точки зрения равновесия, если продукт образуется в заметном количестве. Кроме того, взаимодействие DPNH с красителем ( окислителем) в присутствии диафоразы смещает вправо реакцию лактат - DPN, которая термодинамически менее выгодна. [5]
Дифенил - 1 4-фенилендиамин при окислении также дает две волны; однако продукт первой реакции не устойчив в ацетонитриле. [6]
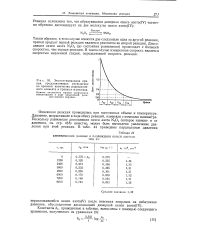 |
Экспоненциальная кривая, представляющая уменьшение во времени количества радиоактивного элемента в процессе а-распада. [7] |
Таким образом, в этом случае имеются две следующие одна за другой реакции, причем продукт первой реакции является реагентом во второй реакции. Диссоциация окиси азота N2O4 ( до состояния равновесия) происходит с большей скоростью, чем первая реакция. В таком случае измеренная скорость является скоростью медленной стадии, определяющей скорость реакции. [8]
При изучении этой реакции было обнаружено, что два грамма исходного эфира дают 1 5 г пикрата продукта первой реакции и 0 3 г продукта второй реакции. [9]
Так, реакции А - В, А - С называются параллельными, а реакции А - В, В - С - последовательными, или консекутивными. В последнем случае продукт первой реакции является исходным веществом для второй. В реакциях полимеризации и других цепных процессах различают стадии инициирования, развития и обрыва цепи. Так, процесс ступенчатой полимеризации описывается следующей простой моделью. Однако образование полимера проходит через ряд стадий. Сначала мономер М активируется катализатором, образуя активный мономер Рг, инициирующий цепь. [10]
Причем даже при избытке меди не вся целлюлоза реагирует во второй стадии реакции. Часть ее остается в растворе в виде продукта первой реакции [ СбН - О2 ( ОН) 2О ] 2 [ Си ( МНз) 4 ] - Количество продукта второй реакции - комплексного соединения [ CeHrOsCuk [ Си ( NN3) 4 ] в соответствии с законом действующих масс увеличивается с увеличением избытка меди в растворе. [11]
Координированный синтез всех ферментов, необходимых для использования того или иного субстрата, дает клетке то преимущество, что она может быстро реагировать на его появление. При последовательной индукции скорость превращения субстрата, а значит, и скорость роста клеток увеличиваются медленно, так как концентрация продукта первой реакции в клетке должна достигнуть определенного порогового уровня, прежде чем она будет стимулировать образование второго фермента. [12]
Первые два его этапа - фосфорилирование молекулы глюкозы и ее дегидрирование до 6-фосфоглюконовой кислоты - идентичны первым двум этапам окислительного пентозофосфатного пути. Специфичны для пути Энтнера-Дудорова две следующие реакции: 1) дегидратирование 6-фосфоглюконовой кислоты, приводящее к образованию КДФГ-кислоты; 2) расщепление продукта первой реакции на два С3 - фрагмента. Конечными продуктами второй реакции являются пировиноградная кислота и 3 - ФГА. Последний окисляется в пировиноградную кислоту так же, как в гликолитическом пути. [13]
В течение нескольких часов скорость поглощения кислорода возрастает, а затем становится практически постоянной, указывая тем самым, что процесс окисления распадается на несколько последовательных реакций. Давидсон предполагает, что имеют место следующие реакции: 1) при первой реакции окисление происходит примерно с постоянной скоростью, 2) происходит окисление продукта, полученного при первой реакции, и номере увеличения количества продукта скорость поглощения кислорода в процессе этой второй реакции также возрастает, 3) наконец, наступает стадия, на которой продукт первой реакции окисляется с такой же быстротой, с какой он образуется, поэтому его количество, а также скорость окисления будут постоянными. Поскольку теперь обе реакции протекают с постоянной скоростью, общая скорость поглощения кислорода будет оставаться постоянной. Аналогичная гипотеза последовательных реакций была выдвинута Бнртуеллом и др. 1203 ] ( гл. [14]
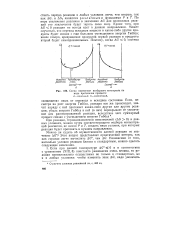 |
Схема изменения изобарного потенциала по мере протекания процесса. [15] |
Страницы: 1 2