Тормозящий продукт
Cтраница 1
Тормозящий продукт, образующийся при окислении, недостаточно эффективен. Окисление проходит довольно глубоко, причем механич. [1]
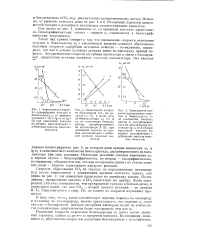
Благодаря образованию тормозящих продуктов, кривые поглощения кислорода при окислении ряда полимеров имеют S-образную форму. Если ур-ние Н. Н. Семенова хорошо описывает лишь начальную стадию разветвленного цепного процесса окисления, то весь процесс может быть описан полуэмпирич. [2]
Замедление реакций распада алканов вдали от равновесных состояний объясняется тем, что крекинг протекает по цепному механизму и замедляется в результате обрыва цепей в объеме на молекулах тормозящих продуктов. Подтверждением этого представления явились опыты по влиянию продуктов распада [48] и обнаружение ингибиторов реакций крекинга - пропилен, изобутилен, аллен, триметил-этилен, N0 и др. [48-50, 54-58, 153], что дало несомненное доказательство цепной природы этих реакций. [3]
Следовательно, и при более высоких давлениях для отражения наблюдаемых в опыте изменений константы скорости с глубиной необходимо учитывать, прежде всего, дезактивацию передатчиков цепей на молекулах тормозящих продуктов крекинга с превращением активных радикалов в неактивные. [4]
Некоторое различие законов изменения w: в первом случае - билогарифмического, во втором - логарифмического, по-видимому, объясняется тем, что при построении кривых не учтено влияние воды - второго тормозящего продукта реакции. [6]
Прежде всего, из формулы ( 36) следует, что для всех алканов, распад которых происходит при помощи одних и тех же активных центров ( Нили СН3, например), а в качестве тормозящих продуктов выступают одни и те же вещества ( например, пропилен или изо-бутилен) и обрыв цепей на стенках происходит с захватом одних и тех же радикалов, р должен иметь одинаковое значение. Действительно, почти одинаковые значения р, найденные в опытах глубокого крекинга различных алканов, подтверждают это, указывая на то, что механизм торможения во всех случаях крекинга одинаковый и основу торможения составляет одна и та же модельная реакция взаимодействия активного радикала с молекулами тормозящего продукта или примеси. Это позволяет сократить проверку полученных соотношений, выполнив ее на примере какого-либо одного алкана, например, пропана. [7]
Уравнение ( 3) следует интерпретировать как зависимость, которая описывает кинетику гетеро-гомогенного радикально-цепного распада, при котором радикалы зарождаются на стенках в условиях адсорбционного, насыщения поверхности, развивают, цепи в объеме и последние обрываются на молекулах тормозящих продуктов и на стенках. Вопреки прежнему толкованию, уравнение ( 3) относится не к гомогенным, а к гетеро-гомогенным реакциям. [8]
Подобный вывод был дан автором в начале 60 - х годов [15] и был основан на анализе радикально-цепной схемы крекинга, в которой зарождение радикалов происходит на стенках в условиях их адсорбционного насыщения молекулами алкана ( концентрация алкана в поверхностном слое постоянная), а обрыв цепей происходит на молекулах тормозящих продуктов гомогенным путем, наряду с обычным обрывом цепей на стенках реактора. [9]
Прежде всего, из формулы ( 36) следует, что для всех алканов, распад которых происходит при помощи одних и тех же активных центров ( Нили СН3, например), а в качестве тормозящих продуктов выступают одни и те же вещества ( например, пропилен или изо-бутилен) и обрыв цепей на стенках происходит с захватом одних и тех же радикалов, р должен иметь одинаковое значение. Действительно, почти одинаковые значения р, найденные в опытах глубокого крекинга различных алканов, подтверждают это, указывая на то, что механизм торможения во всех случаях крекинга одинаковый и основу торможения составляет одна и та же модельная реакция взаимодействия активного радикала с молекулами тормозящего продукта или примеси. Это позволяет сократить проверку полученных соотношений, выполнив ее на примере какого-либо одного алкана, например, пропана. [10]
Общим моментом для формул ( 38), ( 41), ( 42) и ( 44) является входящая в них зависимость от стерического фактора реакции торможения и величины а. Стерический фактор реакции ингибирования с увеличением температуры уменьшается ( см. гл. Вопрос о зависимости а от температуры более сложен. Казалось бы, что с возрастанием температуры должен увеличиваться распад, а, следовательно и концентрация тормозящих продуктов, но изменение температуры может по-разному влиять на соотношение тормозящих и других продуктов распада. Однако, а может оставаться неизменной с изменением температуры. [11]
Страницы: 1