Продукты - первая реакция
Cтраница 1
Продукты первой реакции более устойчивы. [1]
Продукты первой реакции могут быть в большинстве случаев получены и другими методами окисления, а о з о н и д ы являются типичными производными озона. [2]
Продукты первой реакции СО2 и гЬО полностью поглощаются раствором щелочи, поэтому газ, оставшийся после проведения эксперимента - избыточный кислород. [3]
Затем в присутствии катализатора ( порошкообразное железо) кипятят продукты первой реакции, смешанные со второй порцией сероуглерода. Далее четыреххлори-стый углерод отгоняют и направляют на очистку, а остающуюся свободную серу возвращают на производство сероуглерода. [4]
Обратимую реакцию следует рассматривать как две независимые реакции, в которых продукты первой реакции являются исходными - веществами для второй, и наоборот. Стехиометрические коэффициенты прямой и обратной реакций для одного и того же вещества одинаковы, а константы скорости k2 и ks различны. [5]
Если в растворе присутствуют два вещества, реагирующие последовательно с добавляемым реактивом, но продукты первой реакции при данном потенциале окисляются или восстанавливаются на электроде, это мешает получить четкую кривую титрования для второй реакции. [6]
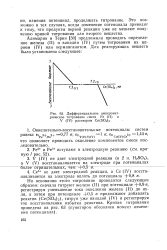 |
Дифференциальное амперомет. [7] |
Это возможно в тех случаях, когда изменение потенциала приводит к тому, что продукты первой реакции уже не мешают получению кривой титрования для второго вещества. [8]
Простейшей реакционной системой является такая, в которой протекает одна-одииствепиая реакция, не усложняемая идущими одновременно с ней вторичными реакциями. Продукты первой реакции могут вступать в дальнейшие реакции, образуя новые продукты. Поэтому обычно изучение кинетики реакций связано со скоростями ряда одновременно протекающих реакций. Задачей химической кинетики является определенно скорости каждой элементарной реакции в ряде одновременно или последовательно протекающих реакций. [9]
Страницы: 1