Распределительный анализ
Cтраница 1
Распределительный анализ представляет собой геометрически дифференциальный анализ, дающий многомерную аналитическую информацию, причем по крайней мере одна пространственная координата пробы принимается за независимую переменную. [1]
Распределительный анализ имеет особое значение при решении материаловедческих и технологических проблем. Он дает важные сведения о распределении элементов на границе зерна, о составе сегрегации в сплавах и об изменениях в пробе, возникших при обработке. Другими важными областями применения являются технология полупроводников, а также биологическое и медицинское исследование и диагностика. [2]
ЭОС является важным методом распределительного анализа элементов. [3]
 |
Схема прибора для обратного рассеяния ионов. [4] |
Обратное рассеяние ионов с хорошо сфокусированными ионными пучками ( ионография) при сравнительно высокой разрешающей способности является эффективным методом распределительного анализа. [5]
Некоторые методы анализа, благодаря весьма высокой геометрической разрешающей способности ( см. табл. 1.9), непосредственно пригодны для распределительного анализа. [6]
Количественное определение пиримидиновых дезоксинуклеозид-3 5 -дифосфатов и низкомолекулярных олигонуклеотидов, освобождающихся из дезоксинуклеиновых кислот при кислотном гидролизе в стандартных условиях ( так называемый метод дифференциального распределительного анализа [411]) с применением поправок на вторичные гидролитические реакции привело к установлению распределения тимина и цитозина. В общем по сравнению с цитозином значительно большая пропорция тимина встречается в виде одиночных звеньев, ограниченных пуриновыми, и около 70 % всех пиримидиновых звеньев присутствует в виде олигонуклеотид-ных участков из трех и более рядом стоящих пиримидинов. [7]
 |
Влияние способа разложения пробы на возможность проведения полного элементного и структурного анализов. [8] |
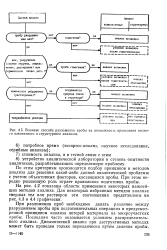
При разложении проб необходимо делать различие между разрушением пробы при подготовительных операциях и предусмотренной принципом анализа потерей материала на микроучастках пробы. Последняя часто оказывается условием распределительного анализа. Динамический анализ при деструктивных методах может быть проведен только периодически путем деления пробы. [9]
Изобразительные способы, например, авторадиография, дают наглядную картину распределения элементов и аналитических неоднородностей в кажущихся макроскопически гомогенными пробах. Методы анализа, применимые для распределительного анализа без разрушения пробы, пригодны почти исключительно для исследования поверхностей и предоставляют данные о верхних атомных слоях, в том числе об адсорбционном слое. [10]
 |
Особенности отбора проб газов и жидкостей. [11] |
Твердые вещества чаще всего оказываются неоднородными. Для определения общего состава ( общий, или валовой, анализ) необходимой предпосылкой является гомогенизация механическим путем или путем растворения. Поэтому микроаналитические методы валового анализа предъявляют особенно высокие требования к гомогенности пробы и, кроме того, делают возможным контроль гомогенности с помощью распределительного анализа. [12]
Степень связывания ионов белками можно определять различными методами; из них наиболее широко распространен метод равновесного диализа. При диализе ( так же как и при осмометрии) используют мешочек, стенки которого непроницаемы для молекул белка, но проницаемы для небольших ионов. Диализный мешочек с раствором белка помещают в раствор, содержащий необходимый ион. После установления равновесной концентрации диффундирующего иона по обе стороны мембраны измеряют концентрацию иона в растворе, не содержащем белка; разность начальной и конечной концентраций иона в не содержащем белка растворе позволяет определить концентрацию иона в растворе белка. Если концентрации иона по обе стороны мембраны равны друг другу, то это означает, что связывания не произошло. Если связывание имело место, то концентрация иона в белковом растворе должна быть выше, чем в растворе, не содержащем белка; разность концентраций может служить мерой числа ионов, связанных с одной молекулой белка. Для того чтобы исключить влияние эффекта Гиббса - Донна-на, равновесный диализ проводят обычно либо в изоэлектрической точке белка, либо при высокой ионной силе. Такие методы, как ультрафильтрация, распределительный анализ, а в некоторых случаях и адсорбционная спектрофотометрия, также могут служить для определения степени связывания ионов с белками. [13]
Страницы: 1