Производство - арсенат - кальций
Cтраница 2
Помимо преимуществ, упомянутых выше, азотнокислотный способ производства арсената кальция имеет еще следующие преимущества перед щелочным ( каталитическим): возможность обойтись без отстаивания суспензии арсената кальция перед фильтрованием; последнее идет в 2 - 3 раза быстрее, фильтровальное полотно разрушается значительно медленнее, а главное, фильтрат и промывные воды полностью возвращаются в процесс. [16]
Каустическая сода, или едкий натр NaOH, применяется в производстве арсената кальция для получения промежуточного продукта - арсенита натрия. Она выпускается в твердом и жидком виде. Твердая каустическая сода представляет собой непрозрачную массу, на воздухе расплывается, поглощая из него влагу. Каустическая сода легко растворяется в воде с выделением тепла, водный раствор ее имеет сильно щелочную реакцию. [17]
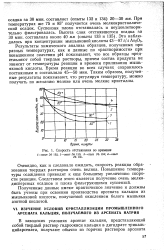 |
Скорость отстаивания во времени. [18] |
Полученные данные имеют практическое значение и должны быть учтены при освоении производства арсената кальция из мышьяковой кислоты, получаемой окислением белого мышьяка азотной кислотой. [19]
В более поздний период был также разработан метод получения арсената кальция окислением белого мышьяка азотной кислотой с нейтрализацией мышьяковой кислоты известью. Производство арсената кальция несколько позднее было также организовано на Константиновском химическом заводе. Однако в связи с низкой эффективностью применения арсената кальция для борьбы с вредителями растений его производство прекращено. [20]
Содержащие ся в техническом белом мышьяке примеси сульфита окисляются до H2SO4 и затем, при нейтрализации, пзрехо-дят в CaSO4, что снижает качество продукта. Поэтому для производства арсената кальция требуется применять белый мышьяк I сорта, содержащий менее 5 % примесей. [21]
Однако скорость окисления 30 - 32 % - ной азотной кислотой мала, и требуется применение катализаторов - НС1, HI. В реакцию вводят 2 - 3 % - ный избыток As2O3, а по окончании окисления оставшийся осадок отделяют и вновь возвращают на окисление. Для производства арсената кальция требуется применять белый мышьяк 1 сорта, содержащий менее 5 % примесей. [22]
Однако скорость окисления 30 - 32 % - ной азотной кислотой мала, и требуется применение катализаторов - НС1, HJ. В реакцию вводят 2 - 3 % - ный избыток As2O3, а по окончании окисления оставшийся осадок отделяют и вновь возвращают на окисление. Для производства арсената кальция требуется применять белый мышьяк 1 сорта, содержащий менее 5 % примесей. [23]
В двух статьях Пирса и Нортона [27], а также Пирса и Эвенса [28] излагаются итоги изучения фазового состава арсената кальция. При 35 были найдены только три из этих соединений [24], основной арсенат кальция отсутствовал. Теперь считается, что последнее соединение составляет главную часть продажного, так называемого безопасного арсената кальция, который в последнее время появился на рынке. Тот факт, что это соединение существует при высокой температуре, имеет большое практическое значение для производства арсената кальция. [24]
В цехе мышьяковистых солей вырабатываются арсенат кальция ( мышьяково-кислый кальций) и парижская ( швейнфурт-ская) зелень. Эти материалы имеют значительную токсичность и применяются в основном для борьбы с сельскохозяйственными вредителями. Ввиду токсичности материалов их транспортирование осуществляется всасывающими пневматическими установками, исключающими запыленность окружающего воздуха. Первые две смонтированы в корпусе производства арсената кальция, остальные - в корпусе производства парижской зелени. [25]
Страницы: 1 2