Сильный окисляющий агент
Cтраница 2
Окисление органического соединения электролитическим методом во многих отношениях очень сходно с действием сильного окисляющего агента. Однако механизм окислительного процесса пока еще окончательно не установлен. Глесстон и Хикклинг предложили механизм [1], согласно которому предполагается, что в водном растворе гидроксильные ионы разряжаются при низком потенциале, образуя гидроксильные радикалы, которые, соединяясь, дают перекись водорода. [16]
Реакция К2 и Вг2 представляет собой крайне интересный пример реакции очень сильного восстанавливающего агента с очень сильным окисляющим агентом. [17]
Реакция может происходить либо с участием гидроксильных радикалов, являющихся промежуточными продуктами, либо в качестве сильного окисляющего агента кислорода. [18]
Реакция может происходить либо с участием гидроксильных радикалов, являющихся промежуточными продуктами, либо с участием в качестве сильного окисляющего агента кислорода. Однако механизм анодного окислительного процесса является очень сложным и пока еще окончательно не установленным, поэтому в каждом отдельном случае необходимо специальное его изучение применительно к исследуемому органическому соединению. При этом, кроме стадий, протекающих на границе раздела фаз ( электрод - раствор), существенное значение имеют химические превращения, совершающиеся в объеме обрабатываемой жидкости. [19]
Анионный обмен, протекающий в нейтральной или щелочной среде, необходим вследствие того, что хромовая кислота является сильным окисляющим агентом. Если бы анионный обмен мог проводиться в растворе хромовой кислоты, проблема очистки значительно упростилась. [20]
Однако янтарная кислота по отношению ко всем органическим окислителям лишь немногим более реакционноспособна, чем уксусная кислота, поскольку она устойчива к таким сильным окисляющим агентам, как хромовая кислота и перман-ганат. [21]
Кроме этого, для некоторых специальных технологических н научных работ имеют большое значение и другие характеристики смол, а именно: механическая прочность и микропорнстость, устойчивость к повышенным температурам, большим дозам радиоизлучений, органическим растворителям н сильным окисляющим агентам. За исключением двух последних все эти факторы изучены достаточно хорошо и результаты исследований могут быть найдены в специальных материалах, касающихся ионообменных смол. [22]
Поведение плутония в разбавленных растворах аналогично поведению нептуния, исключая тот факт, что трехвалентное состояние более стабильно, чем четырехвалентное. Если употребить более сильный окисляющий агент, то плутониевая активность ведет себя так же, как и непту-ниевая. Поскольку окислительно-восстановительный потенциал для пары S04 - j - S2Os равен-2 05 V, а для пары Вг - Вг03 - - равен-1 42 V, то можно ожидать, что окислительно-восстановительный потенциал для пары Ри 4 ЦРиО, должен лежать между ними. [23]
Часто бывает трудно судить о том, происходит ли прямое окисление органического соединения в соответствии с уравнением приведенной выше реакции, или косвенное, вызываемое образованием брома. Поскольку бромат является более сильным окисляющим агентом, нежели бром, постольку считают, что в этом случае более вероятно прямое окисление. [24]
Фторирование мочевин приводит к N. N-дифтормочевинам, которые являются сильными окисляющими агентами, дающими при гидролизе дифторамин. Тетрафтормочевину получают по реакции Г Ы - дифторкарбамоилфторида с фторидом калия. [25]
Хотя многие смолы с высокими эксплуатационными качествами обладают широким диапазоном химической стойкости, улучшение этой характеристики было бы весьма полезным. В частности, было бы желательно создание связующих с улучшенной стойкостью к воздействию органических жидкостей, сильных окисляющих агентов и щелочных растворов высокой концентрации. [26]
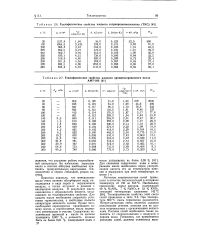 |
Теплофизические свойства жидкого тетракрезилоксисилана ( ТКС.| Теплофизические свойства жидкого ароматизированного масла. [27] |
Расплавы неорганических солей применяют в качестве теплоносителей в интервале температур от 150 до 550 С. Теплофизические свойства этой смеси солей приведены в табл. 2.8. При температуре 800 С смесь термически разлагается. Нитрит-нитратная смесь является сильным окисляющим агентом, поэтому она не должна соприкасаться с органическими веществами. Расплав солей необходимо также защищать от соприкосновения с воздухом и парами воды. [28]
Хорошо известный пример несамовоспламеняющейся двухкомпонент-ной системы, которую было бы заманчиво использовать в качестве основного топлива ввиду широкой доступности и низкой стоимости компонентов, представляет собой система: красная дымящая азотная кислота - бензин. Много растворимых катализаторов воспламенения было разработано для этой системы. Так, прибавление аминов или меркаптанов к бензину и, соответственна, прибавление сильного окисляющего агента, такого, как КМп04, к красной дымящей азотной кислоте дает в результате самовоспламеняющиеся комбинации. Тем не менее активность КМп04, прибавленного к красной дымящей азотной кислоте в качестве катализатора воспламенения, быстро падает со временем в результате осаждения МпОа. Следует ожидать, что дальнейшее применение катализа будет зависеть от открытия более удовлетворительных растворимых катализаторов, нежели имеющиеся в настоящее время. [29]
Расплавы неорганических солей применяют в качестве теплоносителей при нагревании до 550 С. Установки, где применяются расплавы солей, должны отличаться высокой герметичностью и защищаться инертным газом. Смесь применяют при обогреве с принудительной циркуляцией. Нитрит-нитратная смесь является сильным окисляющим агентом, поэтому она не должна соприкасаться с органическими веществами. [30]
Страницы: 1 2