Медленное пропускание
Cтраница 1
Медленное пропускание производится в течение 3 - 4 часов. [1]
Медленное пропускание производят в течение 3 - 4 часов. [2]
Медленное пропускание воздуха производят в течение 3 - 4 часов. [3]
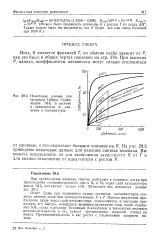 |
Некоторые данные для процесса Габера. Содержание МН3 в системе в зависимости от давления и температуры. [4] |
Однако медленное пропускание газов через слой катализатора неэкономично, и выгоднее пропускать его быстро, возвращая непрореагировавшие газы после отделения NH3 назад в реактор. Основным показателем в технологии является производительность в час, равная произведению скорости потока на выход. Производительность в час растет с увеличением скорости потока. [5]
При медленном пропускании через несколько видоизмененный аппарат Сабатье и Сандерана, при длине слоя никеля в 50 см уже с одного раза происходит почти полная гидрогенизация. Для очистки от следов не вошедшего в реакцию камфена углеводород был растворен в небольшом количестве легкого петро-лейного эфира и подвергнут обработке купоросным маслом до тех пор, пока серная кислота не стала оставаться совершенно бесцветной. Промытый и высушенный раствор изокамфана был подвергнут затем фракционировке. Он очень постоянен по отношению к окислителям; даже азотная кислота уд. [6]
При медленном пропускании газообразного фтора через водный раствор бо-рониевой соли с 40 % - ным выходом получается дизамещенный катион, F2B [ N ( CH3) 3 ] 2; одновременно образуется также монофторированный катион, однако соответствующая соль не была выделена в индивидуальном состоянии. Моно-хлорзамещенные катионы образуются при действии на борониевые соли таких реагентов как SF6C1, NC13 или смеси концентрированных азотной и соляной кислот. [7]
При медленном пропускании тока хлористого водорода при комнатной температуре в, раствор 1 г этилового эфира 5-метил-р - кумаранон-2 - карбоновой кислоты и 1 г резорцина в метиловом спирте происходит постепенное выделение желтого осадка. Через Два дня смесь в течение получаса нагревают на паровой бане, а затем охлаждают; полученный кумарин отделяют, промывают и кристаллизуют из этилового спирта. [8]
Получается при медленном пропускании фтора над сухим селеном ( при комнатной температуре) или при действии трифторида брома на двуокись селе на. [9]
Тетранитрометан получается при медленном пропускании кетена ( полученного пиролизом ацетона) в охлажденную концентрированную азотную кислотг. По окончании реакции масса выливается на лед, и осевший тетранитроыетан отделяют. [10]
Наоборот, при медленном пропускании газа через жидкость улучшаются условия насыщения газовой фазы, но зато ухудшаются условия насыщения жидкой фазы. [11]
Это достигается при очень медленном пропускании водорода через слой окислов в тех случаях, когда реакция имеет значительную скорость. Отсюда следует, что при высоких температурах для восстановления определенного количества кобальта требуется водорода несколько больше, чем при низких температурах. Так как с понижением температуры константа равновесия закономерно увеличивается, можно предполагать, что при температурах ниже 400, например при 200 - 250, восстановление кобальта должно проходить с большим использованием водорода. Однако на практике при этой температуре восстановление не проводят, потому что скорость реакции очень мала. Применение избыточного количества водорода с целью смещения равновесия в сторону восстановления металла дает незначительный эффект и на практике приводит к непроизводительной затрате водорода. Поэтому в целях экономии водорода реакцию восстановления следует проводить, придерживаясь следующего правила: при высоких температурах пропускать водород над окислом с большей скоростью, а при низких температурах, когда восстановление только начинается и скорость реакции мала - с очень небольшой скоростью, но в течение длительного времени. [12]
Очистка хлороформа достигается также медленным пропусканием препарата через колонку, заполненную активным А12О3 в количестве 50 г на 1 л хлороформа. [13]
Сущность процесса состоит в медленном пропускании газа через очистительную массу. [14]
Пирогенетическое разложение2 триэтил-цианурата при медленном пропускании паров в высоком вакууме, над нагретой до красного каления платиновой спиралью, дает циановую кислоту и этилен. Пиролиз идет по нормальному пути разложения этиловых эфиров и характерным для него является то, что обрдзую-щаяся на короткое мгновение циануровая кислота подвергается деполимеризации, что она всегда склонна делать при повышенных температурах. [15]
Страницы: 1 2 3 4