Прикатодное пространство
Cтраница 3
С), так как, по мнению автора указанной работы, в этом случае предотвращается образование основных соединений в прикатодном пространстве, которые обволакивают частицы графита и понижают их самосмазывающие свойства. Снижение-температуры с 20 до 10 С резко повышает ( с 3 9 до 7 4 ГПа) и твердость Fe-покрытий. [31]
Участие катионов электроотрицательных металлов в переносе тока снижает и без того более низкую по сравнению со средней концентрацию меди в прикатодном пространстве, что приводит к росту концентрационной поляризации у катода. [32]
Многочисленные и разнообразные методы кулонометрического титрования кислот и оснований [290, 291, 318, 320, 326, 448, 538, 552-590] базируются на общеизвестном факте, что в ходе электролиза воды в прикатодном пространстве накапливаются ионы ОН -, а в прианодном - ионы Н ( см. стр. Таким образом, разделяя продукты электролиза катодной и анодной камер, можно количественно генерировать титрант для определения кислоты или основания. [33]
Таким образом, наибольшее влияние на содержание железа в сплаве оказывает; по-видимому, при высоких i, в большей степени подщелачивается прикатодное пространство, что благоприятно сказывается на осаждении железа. [34]
Попытки восстановления этих элементов электролизом делались неоднократно, однако, на платиновом электроде идет в первую очередь восстановление водорода, сопровождающееся подтцелачиванием прикатодного пространства, в результате чего РЗЭ выпадают в осадок в виде гидроокисей, которые, как указывалось, весьма мало растворимы. В 1930 г. Интема [763] применил для электролиза РЗЭ ртутный катод, обладающий высоким перенапряжением для выделения водорода, а немного позже Мак-Кой [764] предложил вести электролиз РЗЭ с ртутным катодом в присутствии комплексообразователей - органических кислот, так как в их присутствии РЗЭ при электролизе не осаждаются в виде гидроокиси. С тех пор работы по электролизу РЗЭ с ртутным катодом стали развиваться, тем более что европий, самарий и иттербий восстанавливаются на ртутном катоде не только до двухвалентного состояния, но и до металла, образуя амальгаму. [35]
При плотностях тока, соответствующих первой ветви / - е кривой, видимого выделения водорода и металлического хрома не наблюдалось, рН прикатодного пространства в этом случае не превышало единицы. В данных условиях очевидно, что преобладающим анионом ( см. р ис. [36]
Эта реакция при пропускании тока в 1 F дает столько же водородных ионов, сколько их исчезает за это же время в прикатодном пространстве. Поэтому в этих условиях изменения рН всего раствора не происходит. Если же при анодной реакции не производятся ионы Н или их производится недостаточно для того, чтобы возместить убыль вблизи катода, то при электролизе с течением времени рН раствора постепенно возрастает и продукты гидролиза получают возможность выделяться на катоде. [37]
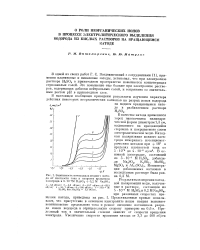 |
Зависимость потенциала медного катода от плотности тока и скорости вращения электрода в 5. ( - % [ H2SOi 0 2 М Na2SO4. [38] |
В одной из своих работ Г. С. Воздвиженский с сотрудниками [1], применяя платиновые и никелевые катоды, установил, что при электролизе раствора H2S04 в прикатодном пространстве повышается концентрация сернокислых солей. Это повышение еще больше при электролизе растворов, содержащих добавки нейтральных солей, и сопряжено со значительным ростом рН в прикатодном слое. [39]
Жданов с сотрудниками [29] показал с помощью метода меченых атомов, что при электролизе водных растворов лан-гана на ртутном катоде амальгама образуется с очень малыми выходами по току вследствие одновременного разряда протонов на катоде и защелачивания прикатодного пространства. [40]
Многочисленные и разнообразные методы кулонометриче - - ского титрования кислот и оснований [ 391, 392, 419, 421, 427, 596, 764, 769 - 833а ] базируются на общеизвестном факте, что в ходе электролиза воды в прикатодном пространстве накапливаются ОН, а в прианодном - Н ( см. стр. Таким образом, разделяя продукты электролиза катодной и анодной камер, можно количественно генерировать титрант для определения кислоты или основания. [41]
Увеличение давления может быть достигнуто или за счет предварительного подогрева газа, или за счет увеличения расстояния между электродом и соплом. Увеличение прикатодного пространства приводит к повышению катодного напряжения и увеличивает нагрев газа в полости сопла, а следовательно, и его давление. [42]
В процессе электролиза хлорид магния разлагается. В прикатодном пространстве ванны выделяется магний, а в анодном - хлор. Магний, как менее плотный, находится на поверхности электролита. Магний по шлангам перекачивают в вакуумный котел, а хлор отсасывают через хлоропровод. Окись магния и частично восстановленное железо оседают на дно ванны в виде шлама, откуда его удаляют черпаками; отработанный электролит удаляют через лейку вакуумными устройствами. [43]
Такая реакция весьма нежелательна, поэтому оба электрода разделяют друг от друга диафрагмой, препятствующей взаимодействию продуктов электролиза. Скопившийся в прикатодном пространстве раствор щелочи периодически спускают, а ванну пополняют новым раствором хлорида. Хлор по трубам подается в расположенные обычно неподалеку цеха для получения хлорной извести. [44]
При работе водородно-водо-родной цепи вследствие окисления водорода на левом электроде и восстановления на правом давление водорода выравнивается. В результате протекания электродных реакций в прикатодном пространстве концентрация катионов уменьшается, а в прианодном - увеличивается, что приводит к возникновению градиента их концентрации, а следовательно, к диффузии. [45]
Страницы: 1 2 3 4