Протекание - указанная реакция
Cтраница 2
Из данных, приведенных в табл. 7, видно, что вероятность протекания указанных реакций большая. [16]
 |
Диффузионный профиль границы раздела эмаль-железо после нагрева при 950 С в течение 10 мин. [17] |
Образование кислородного мостика возможно в момент охлаждения, если скорость охлаждения больше скорости протекания указанной реакции, а также если учесть приток кислорода из атмосферы. [18]
Эти термодинамические данные весьма существенны; кроме того, имеются некоторые качественные экспериментальные доказательства протекания указанной реакции. [19]
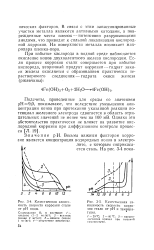 |
Качественная зависимость скорости коррозии стали от рН воды.| Качественная зависимость скорости коррозии стали от рН и температуры. [20] |
Подсчеты, проведенные для среды со значением рН - 9 0, показывают, что вследствие уменьшения концентрации ионов при протекании указанной реакции потенциал железного электрода сдвигается в область отрицательных значений не менее чем на 100 м В. [21]
В зависимости от типа сырья, свойств катализатора, оперативных условий прбцесса, а также от конструктивных особенностей реакционных аппаратов интенсивность протекания указанных реакций может меняться. Проведение процесса в оптимальных условиях заключается в обеспечении максимального протекания желательных реакций при минимуме нежелательных. [22]
Повышенная химическая активность флюса, особенно по кремнезему, приводит к интенсивному протеканию крем-невосстановительного процесса на границе шлак-металл в сварочной ванне, В результате протекания указанной реакции наплавляемый металл одновременно обогащается восстанавливаемым из флюса кремнием и кислородом в виде мелкодисперсных оксидных включений. [23]
 |
Зависимость равновесной концентрации метанола при 350 С от давления и состава исходного газа4. [24] |
В табл. 15 - 17 приведены данные9 о зависимости равновесной концентрации метанола для состава газа, близкого к промышленному ( на цинк-хромовом катализаторе), от давления, температуры к соотношения Н2: СО в циркуляционном газе при условии совмест-лого протекания указанных реакций. [25]
Тот факт, что реакция гомогенного диспропорционирования ионов Си не является одной из стадий анодного растворения меди и не протекает с заметной скоростью, на первый взгляд противоречит широко известному эффекту образования порошкообразной меди в объеме электролита при анодном растворении меди, поскольку этот эффект обычно объясняют именно протеканием указанной реакции. Действительно, каждую такую частичку ( или зародыш) можно рассматривать как обесточенный электрод, находящийся в растворе с повышенной концентрацией одновалентных ионов, и поэтому к ним применимы все рассмотренные и полученные выше закономерности. [26]
Бариевые соли сульфаминовых кислот растворимы в воде. Поэтому протекание указанной реакции в присутствии ионов бария приводит к образованию осадка сульфата бария. Это может быть положено в основу надежной реакции обнаружения соединений этого класса. [27]
Если в протекании указанных реакций образуются в качестве промежуточных соединений ацетиленовые или алленовые углеводороды, то их изомеризация в диеновые должна осуществляться через перемещение атомов водорода от метиленовых групп, стоящих в а - или р-паложении к углеродным атомам, к которым перемещаются водородные атомы. [28]
Промотирование алюмоплатинового катализатора рением способствует также значительному повышению его активности в реакциях гидрогенолиза. Для подавления скорости протекания указанной реакции катализатор подвергают дозированному осернению, при этом металлические центры, катализирующие гидрогенолиз, отличаются и наибольшей активностью в адсорбции серы. [29]
Значения & Z 9S, вычисленные нами и приведенные выше, для всех реакций являются положительными. Это свидетельствует о невозможности протекания указанных реакций при температуре 598 К, а следовательно, и об отсутствии сил химической связи между покрытиями и металлом. [30]
Страницы: 1 2 3