Неполное протекание - реакция
Cтраница 1
Неполное протекание реакции объясняется обволакиванием непрореагировавшего флюорита выделяющимся ангидритом и трудностью равномерного смешения флюорита с серной кислотой. [1]
Вследствие неполного протекания реакции бромата калия с ок-симом в интервале температур 16 - 30 С для расчета используют эмпирический коэффициент К ъ установленный для этого интервала температур. [2]
В действительности выходы продуктов вследствие неполного протекания реакций и потерь бывают ниже, чем по теории. Практические выходы принято выражать в процентах от теоретических выходов. [3]
В реальных химических процессах из-за неполного протекания реакции и различных потерь веществ масса образующихся продуктов часто бывает меньше той, которая должна образоваться в соответствии с законом сохранения массы веществ. [4]
В условиях калориметрического эксперимента это приводит к неполному протеканию реакции взаимодействия компонентов. Чувствительность метода микрокалориметрии позволяет работать с концентрациями меньше 0 001 моль / л, однако при этом значительно возрастает ошибка эксперимента, связанная с приготовлением растворов и влиянием сравнимых концентраций примесей. [5]
Низкое значение константы равновесия означает наличие в растворе исходных веществ вследствие неполного протекания реакции. [6]
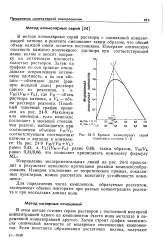 |
Кривая изомолярных комплекса состава 1. 2. [7] |
Искривление экспериментальных линий на рис. 24 - 9 происходит в результате неполного протекания реакции комплексообра-зования. Измеряя отклонение от теоретических прямых, показанных пунктиром, можно рассчитать константу устойчивости комплекса. [8]
Фридман и Ирза [700] исследовали ошибки, вызываемые фракционированием изотопов водорода, связанные с неполным протеканием реакции. [9]
Метод абсолютной калибровки обладает преимуществом в тех случаях, когда необходимо устранить ошибки, вызываемые неполным протеканием реакции или потерями при подготовке пробы до введения в прибор. Далее, при этом уменьшаются ошибки, вызываемые высокой асимметрией пиков, частично необратимой сорбцией, частичным разложением или нелинейностью показаний детектора. Это правильно лишь в том случае, если калибровочная кривая строится при применении в качестве стандарта чистого вещества, представляющего аналитический интерес. Если должны устраняться ошибки, возникающие во время обработки пробы до хроматографии, то необходимо, чтобы пробы для калибровки обрабатывались тем же методом, что и анализируемые пробы. [10]
Визуальное определение конечной точки титрования возможно не всегда - иногда из-за отсутствия пригодного индикатора, иногда вследствие неполного протекания реакции между титруемым веществом и титрантом. В таких случаях несомненными преимуществами обладают физико-химические методы индикации. Кроме того, они находят все более широкое применение потому, что некоторые из них, можно полностью автоматизировать. [11]
Визуальное определение конечной точки титрования возможно не всегда - иногда из-за отсутствия пригодного индикатора, иногда вследствие неполного протекания реакции между титруемым веществом и титрантом. В таких случаях несомненными преимуществами обладают физико-химические методы индикации. Кроме того, они находят все более широкое применение потому, что некоторые из них можно полностью автоматизировать. [12]
Использование бензилхлорида дает во многих случаях адекватные результаты, но отмечены и случаи их занижения, возможно, из-за неполного протекания реакции бензилхлорида с литийорга-ническим соединением. [13]
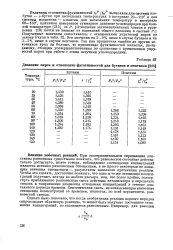 |
Давление паров и отношение фугативностей для бутанов и пентанов. [14] |
При экспериментальном определении константы равновесия существенно показать, что равновесное состояние действительно достигнуто, иначе говоря, наблюдаемое соотношение концентраций является истинно равновесным отношением, а не просто некоторым не имеющим значения отношением - результатом неполного протекания реакции. Чтобы это сделать, достаточно показать, что одно и то же отношение концентраций получают, исходя из любого изомера, или, что более удобно, подвергнуть приближенно равновесную смесь действию катализатора и определить степень и направление изменения отношения концентраций в течение длительного периода времени. Синтетическая смесь, не показывающая изменение отношения концентраций со временем, является, но всей вероятности, равновесной смесью. [15]
Страницы: 1 2