Спокойное протекание - реакция
Cтраница 1
Спокойное протекание реакции между боргидридом натрия и серной кислотой обеспечивается за счет добавки к ней модераторов, например, антрахинона или антрахинонсульфокислоты ( до 10 вес. [1]
Достоинствами электрохимического способа фторирования являются спокойное протекание реакции и лозможпость ее регулирования. Однако достигаемые выходы фторпроизводных пока недостаточно высоки. [2]
 |
Фуроксаны АгСО - CjNjC - СОАг, полученные из арнлметилкетонов нитрованием смесью разбавленной азотной и уксусной кяслот. [3] |
Снайдер и Бойер [536] пришли к заключению, что замена концентрированной азотной кислоты иа разбавленную ( - 20 % - ную) способствует еще более спокойному протеканию реакции, как правило, без существенного изменения выхода. Для создания начальной концентрации нитро-зирующего агента в нитрующую смесь добавляют несколько кристаллов нитрита натрия. Температуру реакционной смеси устанавливают в зависимости от строения кетона, но обычно не выше [ 00 С. Реакция протекает спокойно, с медленным выделением окислов азота. [4]
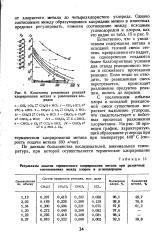 |
Константы равновесия реакций хлорирования метана и разложения хло -. ридов. [5] |
Естественно, что с увеличением содержания метана в исходной газовой смеси степень превращения его падает, но одновременно создаются более благоприятные условия для отвода реакционного тепла и спокойного протекания реакции. Если тепло не отводить, то реакционная смесь перегревается, происходит разложение продуктов реакции, вплоть до взрывов. [6]
Белый фосфор растворяют в малогорючем 1-хлорнафталине и добавляют стехиометрическое количество серы. Растворитель способствует более спокойному протеканию реакции и служит средой для кристаллизации сульфида. По окончании реакции смесь охлаждают при перемешивании. Большая часть Р4 з выпадает в виде мелкого порошка. [7]
Арсенид галлия рекомендуется растворять при нагревании в смеси 8 М хлороводородной кислоты, брома и четыреххлори-стого углерода. Четыреххлористый углерод разбавляет бром и тем самым способствует спокойному протеканию реакции. [8]
Реакцию проводят при 240 - 250 С и давлении до 70 ат. Применяя хорошее перемешивание, можно достичь высокой дисперсности натрия и обеспечить спокойное протекание реакции. После отгонки растворителя получается порошкообразный триметоксиборгидрид натрия. [9]
Движущийся теплоноситель и ступенчатый ввод хлора являются, очевидно, решающими факторами, обеспечивающими спокойное протекание реакции при таком глубоком хлорировании пропана. [10]
Меняя соотношение, а иногда и условия реакции, можно синтезировать преимущественно то или другое соединение. Естественно, что с увеличением содержания метана в исходной газовой смеси степень превращения его падает, но одновременно создаются условия для отвода реакционного тепла и спокойного протекания реакции. Если тепло не отводить, происходит разложение продуктов реакции вплоть до взрыва. [11]
Показания термопар 22 и 23 позволяют достаточно точно определять скорость пиролиза, происходящего в зоне восстановления. Желательно, чтобы температура находилась в пределах от 700 С в нижней части зоны 6 до 200 С в верхней части зоны восстановления, что обеспечивает спокойное протекание пиролитической реакции без уноса серебра с отходящими газами. [12]
Однако ранние наблюдения ( Дэви, Бертло, Велер) свидетельствовали о взрывном характере прямого присоединения хлора к ацетилену, поэтому последующие работы развивались по двум направлениям: 1) выяснение причин, вызывающих взрыв смеси ацетилена с хлором [193, 297-300]; 2) поиски веществ, способных обеспечить спокойное протекание реакции. [13]
При обычных температурах в темноте хлор и водород не взаимодействуют. На свету или при нагревании реакция в смеси этих газов сопровождается взрывом. Спокойное протекание реакции между хлором и водородом ( без взрыва) возможно при непрерывном поступлении газов в реакционную зону и высокой температуре ( обычно 2000 - 2400 С), которая поддерживается за счет выделения реакционного тепла. Реагирующие газы образуют светящийся факел бледно-лунного цвета. [14]
При обычных температурах в темноте хлор и водород не взаимодействуют. На свету или при нагревании реакция в смесл этих газов сопровождается взрывом. Спокойное протекание реакции между хлором и водородом ( без взрыва) возможно пои непрерывном поступлении газов в реакционную зону и высокой температуре ( обычно 2000 - 2400 С), которая поддерживается за счет выделения реакционного тепла. Реагирующие газы образуют светящийся факел бледно-лунного цвета. [15]
Страницы: 1 2