Енольный протон
Cтраница 1
Наблюдаемое деэкранирование енольного протона и трифторацетильной группы ( в спектрах 19F) с увеличением электронодонорности заместителя X указывает на увеличение доли енола ( ПБ), т.е. о присутствии в растворе обеих цис-енольных форм. [1]
Наблюдаемый химический сдвиг енольного протона 8ОН зависит как от химического сдвига енольного протона в каждой форме, так и от относительного содержания этих форм. [2]
Константы 13С, Н дальнего спин-спинового взаимодействия енольного протона в спектрах высокого разрешения ЯМР 13С 2-ацетилдимедона / / Докл. [3]
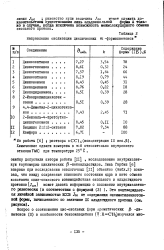 |
Направление енолизации циклических ос - формилкетонов. [4] |
А только в случае, когда исключена возможность межмолекулярного обмена енольного протона. [5]
Наблюдаемый химический сдвиг енольного протона 8ОН зависит как от химического сдвига енольного протона в каждой форме, так и от относительного содержания этих форм. [6]
Однозарядный анион ацетил ацетон а СНзСОСШСОСНз ( образованный отщеплением одного из енольных протонов) реагирует со многими ионами металлов, образуя нейтральные комплексы. Аналогичные комплексные соединения его производного - а-теноилтрифторацетона CXXV - экстрагируются бензолом гораздо легче, что связано с наличием в нем тиофенового ядра. [7]
В качестве примеров бидентатных лигандов можно указать на изомеры хелатированного амида глицина, координированного по атому азота или кислорода, который найден в [ Co ( en) 2 ( glyam) ] 3 ( CIV CV) ( для последнего рКа енольного протона равен примерно 0 4), а также на своеобразный комплекс CVI, в котором предполагают наличие двух хелатных колец различного размера в одном и том же лиганде. [8]
Отсутствие в ИК-спектре 57 поглощения ОН-группы в области 3000 - 3600 см 1 и аномально слабопольный сдвиг сигнала енольного протона в спектре ЯМР Н свидетельствовали об этом. [9]
Сначала спектр ЯМР содержит в основ - ном линии транс-енольной формы ( IA), в частности дублет гидросильных протонов в высоких полях. Уменьшение интенсивности линий форш ( IA) и рост новых сигналов указывает, что со временем ( IА) переходит через альдо-форму ( 1Б) в цис-енол ( IB), дублет енольных протонов которого расположен в низких полях. [10]
Как отмечено ранее, заместитель. ОГ КСГ3) Нам представляется возможным следующее объяснение наблюдаемого явления. При переходе от электроноакцепторных к электронодонорным заместителям электронная плотность на бензоильном атоме кислорода форм ( II Б) увеличивается по-видимоыу, в большей степени, чем на формильном ( ацетильном, трифторацетильном) атоме кислорода форм ( НА), в то время, как заряды на енольных атомах кислорода обеих форм не должны изменяться сколько-нибудь значительно ввиду отсутствия сопряжения. Следует отметить, что химический сдвиг енольного протона & оя меняется симбатно с остальными спектральными параметрами ( 6ча, / щ, , 7ае), что подтверждает наше предположение [ 2l ] o возможности использования этого параметра для определения направления смещения внутрихелатного равновесия. [11]
Страницы: 1