Протонирование - амид
Cтраница 1
Протонирование амида по атому кислорода стабилизировано сопряжением. [1]
Протонирование амидов изучалось во многих работах и подробно здесь рассматриваться не будет. Полученные результаты позволяют сделать вывод, что у амидов в неводных кислых растворах протонируется в основном атом кислорода. [2]
Предельная степень протонирования амидов и пептидов сильными кислотами остается невыясненной. Равновесие в реакции протонирования азота, описываемой уравнениями ( 13.13 а) и ( 136), несомненно, сдвинуто влево. Однако убедительно показано, что в определенных условиях происходило протонирование пептидного кислорода, ка. Методами криоскопии [101] и УФ-апектросколии [98, 105, 107] было с очевидностью продемонстрировано практически полное протонирование различных амидов в 100 % - ной серной кислоте. Например, сигнал N-метильной группы N-метилацетамида в серной кислоте представляет собой нормальный дублет. Если бы в системе происходило протонирование по азоту [ см. уравнение ( а) ], то этот сигнал должен был бы быть триплетом или, в случае быстрого обмена с растворителем, синглетом. [3]
Частичный положительный заряд, возникающий на атоме азота, настолько снижает основность, что протонирование амидов ( заметное только в сильнокислой среде) осуществляется по атому кислорода. В этом случае заряд образующегося катиона может делокализоваться в отличие от альтернативного азот-протонированного катиона, где делокализация невозможна. [4]
Из-за очень интенсивной делокализации в CONH2 - rpynne основные свойства азота в весьма значительной степени перенесены на кислород, и данные ЯМР-спектров показывают, что протонирование амидов происходит по атому кислорода. [6]
В этом случае обычно образуется смесь О - и N-алкили-рованных изомеров ( 96) и ( 97) Попытки объяснить соотношение изомеров, полученное в нейтральных условиях [252], на основании амбидентной. Факт первоначального образования О-алкильного продукта, согласующийся с местом протонирования нейтральных амидов ( см. разд. О и N соответственно схемы ( 132) и ( 133), предполагают, что ( 99) обладает более низкой энергией, так как делокализация неподе-ленной пары электронов азота уменьшает положительный заряд. [7]
 |
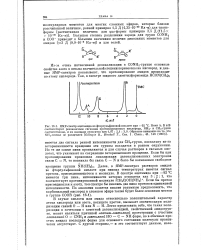
Расчетная зависимость константы скорости гидролиза бензамида от концентрации серной кислоты и экспериментальные значения констант ( О. [8] |
Такие же экстремальные зависимости характерны для гидролиза некоторых амидов и сложных эфиров. Левее максимума ( рис. 40) скорость растет с увеличением кислотности из-за повышения степени протонирования амида. Правее максимума скорость гидролиза снижается с ростом кислотности из-за уменьшения концентрации свободной воды в результате ее протонирования и концентрирования кислоты. Степень протонирования амида при этом близка к количественной. [9]
Хотя катализируемый основанием гидролиз амида протекает, как полагают, по пути ( а) ( см. ниже), катализируемый кислотой гидролиз может быть представлен схемами ( б) или ( в), отличающимися местом первоначального протонирования. Вполне вероятно, что оба механизма осуществляются параллельно в тех случаях, когда атом азота обладает достаточно заметной основностью и энергии активации для обоих направлений сравнимы ( см., однако, замечания о протонировании амидов, гл. [10]
Хотя катализируемый основанием гидролиз амида протекает, как полагают, по пути ( а) ( см. ниже), катализируемый кислотой гидролиз может быть представлен схемами ( б) или ( в), отличающимися местом первоначального протонирования. Вполне вероятно, что оба механизма осуществляются параллельно в тех случаях, когда атом азота обладает достаточно заметной основностььэ и энергии активации для обоих направлений сравнимы ( см., однако, замечания о протонировании амидов, гл. [11]
Соединение C10H13NO: ИК-спектр имеет карбонильную полосу амидного типа вблизи 1680 см-1 и две полосы в области 3300 - 3400 см-1, обусловленные группой CONH. В ЯМР-спектре имеются сигналы пяти типов протонов с соотношением интенсивностей 1: 5: 2: 2: 3 и с химическими сдвигами, указывающими на наличие амидного, фенильных, метиленовых и СОСНз-протонов. Сигнал, обусловленный водородами метиленовой группы, усложняется за счет спин - спинового расщепления протонами соседних атомов углерода и азота. Если протонирование амидов происходит по азоту, делокализация электронов в амндной структуре становится невозможной; в этом случае будет происходить свободное вращение вокруг свяэи С - N. N-диметилформа-мида это приведет к тому, что N-метильные группы станут магнитно эквивалентными и в ЯМР-спектре будет присутствовать синглет протонов обеих метальных групп. [12]
Такие же экстремальные зависимости характерны для гидролиза некоторых амидов и сложных эфиров. Левее максимума ( рис. 40) скорость растет с увеличением кислотности из-за повышения степени протонирования амида. Правее максимума скорость гидролиза снижается с ростом кислотности из-за уменьшения концентрации свободной воды в результате ее протонирования и концентрирования кислоты. Степень протонирования амида при этом близка к количественной. [13]
Продолжается дискуссия по вопросу о том, включает ли эта медленная стадия образование тетраэдрического интермедиата из О - сопряЖенной кислоты или происходит прямое ( SN2) замещение N-сопряженной кислоты, или возможно имеет место комбинация и того и другого. Большая часть из недавно опубликованных фактических данных говорит в пользу направления, в котором участвует О-сопряженная кислота. К ним относятся: относительные скорости превращения N-ацетилпирролидина и пиперидина [226], а также структурно близких амидов и эфиров имидатов [ 227; наблюдения об очень незначительном, но измеримом конку-рентнчом обмене 130 для бензамидов [228] и данные [229] о низких скоростях реакций N-сопряженных кислот при исследовании N-ацетилтриалкиламмониевых, солей. В этой ра - боте приводятся также данные о ранее опубликованных альтернативных интерпретациях корреляций функций кислотности. Хотя механизм может быть спорным, нет сомнений в том, что скорости гидролиза большинства амидов проходят через максимум, положение которого зависит от структуры кислоты и амида. Этот максимум обычно составляет около 2 - 5 М для H2SOi, что соответствует 100 % протонирования амида, и наблюдаемое уменьшение скорости связано с уменьшением активности воды. Сделано много попыток определить роль воды в этих реакциях путем корреляции скоростей реакции с функциями кислотности ( а и Я0) и с близкими данными. Такие сопоставления, проведенные в работах [230, 231], ввиду их важности требуют выбора механизма реакции, однако во всех случаях предполагается наличие в высокой степени сольватированного переходного состояния. [14]
Страницы: 1