Протонирование - спирт
Cтраница 1
Протонирование спиртов в ненуклеофильной среде приводит в конечном итоге к дегидратации. Дегидратация спиртов происходит при нагревании в концентрированной серной кислоте, фосфорной кислоте или в суперкислой среде - смеси пятифгористой сурьмы и фторсульфоновой кислоты. Катион алкоксония в результате отщепления воды образует карбокатион в качестве нестабильного интермедиата. В ненуклеофильной среде карбокатион теряет протон с образованием алкенов. [1]
Протонирование спиртов в ненуклеофильной среде приводит в конечном итоге к дегидратации. Дегидратация спиртов происходит при нагревании в концентрированной серной кислоте, фосфорной кислоте или в суперкислой среде - смеси лятифто-ристой сурьмы и фторсульфоновой кислоты. Катион алкоксония в результате отщепления воды образует карбокатион в качестве нестабильного интермедиата. В ненуклеофильной среде карбокатион теряет протон с образованием алкенов. [2]
Реакция начинается с протонирования спирта. [3]
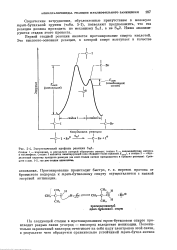 |
Энергетический профиль реакции SN.. [4] |
Первой стадией реакции является протонирование спирта кислотой. [5]
Эта стадия происходит сразу же после протонирования спирта, потому что в результате образуется стабильный катион. На третьей стадии этот катион атакуется бромид-ионом. [6]
При разложении ионов оксония, образующихся при протонировании спирта или эфира, отщепление карбониевого иона может быть предпочтительным процессом. [7]
Поскольку энергия активации для обратной реакции составляет примерно 21 ккал / моль, то написанная реакция должка иметь энергию активации около 37 ккал / моль и оказывается слишком медленной, чтобы возможно было измерить ее скорость. Протонирование спирта улучшает свойства уходящей группы, поскольку в этом случае отщепляется вода, почти столь же хорошая уходящая группа, как и бромид-ион. Практически это выражается в том, что первичные спирты можно превратить в алкилбромиды нагреванием спирта с бромидом натрия и серной кислотой. Способность к замене атомов галогена повышается координацией с ионами металлов, и обычно на практике в качестве катализаторов в реакциях замещения алкнл-галогенидов используют серебряные соли. [8]
Процесс осуществляют также каталитическим путем - пропуская аммиак и соответствующий спирт над А12О3 при 300 С. Катализ, очевидно, сводится к протонированию спирта активными гидроксильными группами, имеющимися на поверхности катализатора, и реакция протекает, следовательно, по той же схеме, что и в кислой среде. [9]
По аналогичному механизму происходит обратная реакция - замена гидро-ксильной группы на галоген, например при взаимодействии трет - - бутилового спирта с концентрированной бромоводородной кислотой. Однако в этом случае, как и в реакции типа 5 2, нуклеофнльному замещению предшествует быстрое протонирование спирта, необходимое для превращения плохо уходящей группы НО - в хорошо уходящую группу - молекулу воды. [10]
Страницы: 1