Процент - обмен
Cтраница 1
Процент обмена как функция числа введенных атомов D сначала падает, затем повышается, достигая максимума на пяти атомах D, а затем доходит почти до нуля на шести атомах, после чего снова начинает возрастать. Разрыв кривой между пятью и шестью атомами, следует думать, происходит вследствие десорбции молекулы после обмена пяти атомов и последующей адсорбции ее второй стороной кольца. Эффект ослабляется с повышением температуры; для циклогексана он меньше, чем для циклопентана, а для циклогептана еще меньше. [1]
Под процентом обмена подразумевается процентное содержание изотопов водорода в газовой фазе. За исключением некоторых опытов, в которых скорость реакции изучалась как функция времени, все реакции проводились в течение 5 мин. [2]
Найдена зависимость процента обмена от концентрации серы в сероуглеродном растворе. [3]
 |
Схема счетной установки. [4] |
Доля обмена, или процент обмена, характеризуют распределение активности между двумя фазами после окончания обмена или через какой-то определенный промежуток времени. Число атомных слоев определяется измерением величины активности в первоначально неактивной фазе через какой-то промежуток времени обмена с последующим пересчетом на вес обменявшегося металла или на глубину захватываемого обменом металла при известной величине поверхности. [5]
В табл. 3 приведены величины процента обмена как функции времени, а в табл. 4 - как функции давления. [6]
К - константа скорости; т-время обмена; А - равновесный процент обмена. [7]
Аналогичным образом определяется среднее время занятия на один вызов и при другом проценте транзитного обмена. [8]
Аналогичным образом определяется среднее время занятия ВРКШ на один вызов и при другом проценте транзитного обмена. [9]
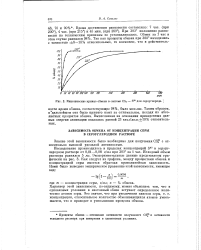 |
Кинетические кривые обмена в системе CSa. [10] |
Таким образом, в дальнейшем оно было принято нами за оптимальное, исходя из абсолютных процентов обмена. Вычисленная на основании приведенных данных энергия активации оказалась равной 23 ккал / молъ 10 % относительных. [11]
Для выражения своих результатов Кольтгоф и его сотрудники не пользуются такими общепринятыми величинами, как доля или процент обмена, а используют для этой цели следующие величины, применимые в тех случаях, когда все количество меченых атомов первоначально находилось в растворе. [12]
Как следует из рис. 113, гидроксильные группы, которым соответствует высокочастотная полоса ( 3785 см-1), обмениваются быстрее других. Установлено линейное соответствие между величинами процента обмена и логарифмом времени обмена. Нанесение на, [ Поверхность окиси алюминия платины приводит к увеличению скорости обмена. Авторы считают, что различие результатов их исследования скорости обмена с результатами работы [1], в которой наблюдался более быстрый обмен гидроксиль-ных групп, соответствующих низкочастотной полосе поглощения, может объясняться различием в кристаллографической структуре исследованных образцов окиси алюминия и в температуре обмена. Однако в работе [5] найдено, что и в случае Y-ОКИСИ алюминия гидроксильные группы, соответствующие высокочастотной полосе поглощения 3785 см-1, обмениваются с D2 наиболее быстро. [13]
Методом изотопного обмена показано [462, 463], что полнозамещенные соединения ртути обменивают свои радикалы с органическими соединениями натрия, магния, цинка, алюминия, кремния и олова. Так, диэтилртуть [462] реагирует со следующими этильными соединениями металлов, содержащими этильную группу, меченную С14 ( в скобках условия реакции и процент обмена): C2H6Na ( комн. Диэтилртуть, содержащая С14, тоже реагирует с диэтилцинком ( 65 С; 20 час. Но между ( CD8) 2Hg и ( CH3) sCd или ( CH3) 2Zn, [ 361а ], а также между ( CH3) 2Hg и ( CHa) aCd или ( CH8) aZn, как показано [ 368а ] методом ядерного магнитного резонанса, обмена радикалами не происходит. [14]
В первом за 68 ч обмен в метильной группе достигает 30 % от равновесного в щелочном растворе и не идет в кислом, а во втором - тот же процент обмена за то же время достигается уже в нейтральном растворе и увеличивается до 60 % в щелочном. Отсутствие обмена с ядерными водородными атомами было доказано окислением группы СН3 у 2 4-динитротолуола, после чего полученная динитробензойная кислота оказалась свободной от дейтерия. Таким образом, обмен локализован в метильной группе, ионизация которой облегчается присутствием нитро-групп, оттягивающих от нее электроны. [15]
Страницы: 1 2