Процесс - диссоциация - комплекс
Cтраница 1
Процесс диссоциации комплексов и процесс восстановления металла может и не быть обратимым. [1]
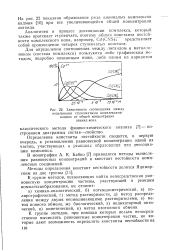 |
Зависимость соотношения между. [2] |
Аналогичен и процесс диссоциации комплекса, который также протекает ступенчато, поэтому общая константа нестойкости комплексного иона, например, Cd ( CNS) 4 - представляет собой произведение четырех ступенчатых констант. [3]
Аналогичен и процесс диссоциации комплекса, который также протекает ступенчато, поэтому общая константа нестойкости комплексного иона, например Cd ( CNS), представляет собой произведение четырех ступенчатых констант. [4]
При повышенных температурах процесс диссоциации комплексов может осуществляться за счет энергии тепловых флуктуации. В этом отношении процесс диссоциации комплексов в ионных кристаллах аналогичен процессу электролитической диссоциации солей, кислот или оснований, хорошо известному из электрохимии растворов электролитов. [5]
Стандартные значения теплот и энтропии процессов диссоциации комплексов ZrClj - POCI3 и НЮ14 - РОС13 представлены в табл. 10 и И. [6]
Рассмотренный метод был использован В. И. Кравцовым и Л. Я. Смирновой при изучении процессов диссоциации комплексов PtC. [7]
 |
Схема реакции кислот с ЭДА ( R - алкильный радикал Ci - С28.| Схема реакции кислот с ДЭТА ( R - алкильный радикал Ci - С2в 23 - 472 35. [8] |
Причем, если при нормальном давлении идет межмолекулярная реакция замещения по углеродному атому карбоксильной группы с образованием моно - и диаминов, то в вакууме скорость процесса диссоциаций комплексов ( II, а; II, б) повышается, в результате чего равновесие в большей степени сдвигается в сторону протекания внутримолекулярной реакции по мезомерному атому углерода амидной. [9]
Простейшая предшествующая электродная реакция замедленной диссоциации была впервые полярографиче-ски изучена рядом авторов [25 - 27], однако подробное кинетическое решение для последовательной многоступенчатой реакции диссоциации с одной замедленной стадией дано в работах Корыты [28] применительно к процессам диссоциации комплексов металлов. [10]
При повышенных температурах процесс диссоциации комплексов может осуществляться за счет энергии тепловых флуктуации. В этом отношении процесс диссоциации комплексов в ионных кристаллах аналогичен процессу электролитической диссоциации солей, кислот или оснований, хорошо известному из электрохимии растворов электролитов. [11]
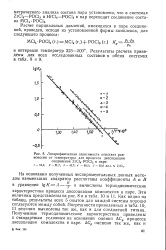 |
Логарифмическая зависимость констант равновесия от температуры для процесса диссоциации соединения ZrCl4 - POCl3 в паре. [12] |
Эти величины представлены на рис. 8 и в табл. 10 и И. Как видно из таблиц, результаты всех 5 опытов для каждой системы хорошо согласуются между собой. Погрешности приведенных в табл. 10, 11 величин вычислены так же, как и для соединений титана. Полученные термодинамические характеристики приведены к стандартным условиям на основании оценки АСр процесса диссоциации комплексов в паре. [13]
Страницы: 1