Процесс - коррозия - железо
Cтраница 1
Процесс коррозии железа может идти очень быстро, потому что образующийся при этом рыхлый слой ржавчины не предохраняет металл от дальнейшего разрушения. [1]
Процесс коррозии железа может идти очень быстро, потому что образующийся при этом рыхлый слой ржавчины и не предохраняет металл от дальнейшего разрушения. [2]
Процесс коррозии железа может идти очень быстро, потому что образующийся при этом рыхлый слой ржавчины не предохраняет металл от дальнейшего разрушения. [3]
Схема протекания процесса коррозии железа во влажном воздухе, загрязненном хлороводородом, аналогична схеме, изображенной на рис. 102, только со следующими отличиями: анодом ( разъедаемыми участками) являются участки, лишенные естественной окисной пассивирующей пленки, а катодом - участки, покрытые пленкой. Коррозия протекает в пленке влаги, адсорбированной поверхностью ме1 - талла и содержащей растворенный кислород. [4]
Установлено, что процесс коррозии железа в расплавленных карбонатах лития и калия протекает в диффузионном режиме в несколько стадий. При этом на поверхности металла накапливаются оксидные и солевые пленки, образующиеся из продуктов коррозии. Обнаружено, что скорость коррозии уменьшается со временем за счет образования на поверхности металла оксидов и малорастворимых в расплавленном карбонате ферритов. С увеличением температуры скорость коррозии возрастает. При увеличении продолжительности эксперимента скорость коррозии стремится к постоянному значению. Энергия активации коррозионного процесса равна 3.168 ккал / моль. Коррозия железа в расплаве карбонатов определяется растворимостью оксидных и солевых пленок, покрывающих поверхность металла, сцеплением их с основой и скоростью диффузии через пленку окислителей и ионов металла. Толщина пленок, составляющая Юмкм, растет с увеличением температуры и временем выдержки в расплаве. Отмечено уменьшение стационарного потенциала железа с ростом температуры в связи с понижением вязкости расплава. Введение карбоната кальция в расплав способствует понижению стационарного потенциала вследствие образования малорастворимого феррита кальция. [5]
Полагают, что ингибирование процесса коррозии железа хроматами является частично катодным13; по-видимому, смешанные окислы железа и хрома, упрочняющие окисную пленку, образованную на воздухе, имеют пониженную электронную проводимость по сравнению с первоначальной окисной пленкой. [6]
Однако механизм стимулирующего действия сероводорода в процессе коррозии железа не может считаться окончательно выясненным, поскольку известны случаи, особенно в практике нефтедобывающей и нефтеперерабатывающей промышленности, когда скорость коррозии металла оказывается значительно большей, чем можно было ожидать. [7]
Полагают, что эти соединения в процессе коррозии железа или стали в той или иной степени восстанавливаются и разлагаются с образованием сульфидов и ионов HS7 Поэтому их адсорбцию и ингибирутршее действие и в данном случае можно связать с предварительной адсорбцией ионов Н5 - на поверхности металла. [8]
Некоторые органические вещества, не влияющие на процесс коррозии железа в нейтральных средах, становятся эффективными ингибиторами при наложении катодной поляризации. [9]
Таким образом, ионы хлора участвуют в процессе коррозии железа многократно, и чем полнее протекает гидролиз, тем больше образуется солей железа. [10]
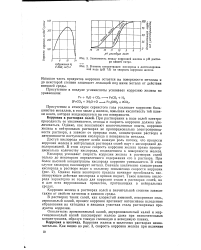 |
Зависимость между коррозией железа и рН раствора едкого натра. с ч.| Влияние концентрации кислорода в дистиллированной воде ( рН 7 0 на скорость коррозии железа. [11] |
Доступ кислорода играет особо важную роль потому, что процессы коррозии железа в нейтральных растворах солей идут с кислородной деполяризацией. В этом случае скорость коррозии железа прямо пропорциональна количеству кислорода, подведенного к поверхности железа. [12]
Мы предполагаем следующую схему действия сульфатов натрия, калия и кальция в качестве ускорителей процесса коррозии железа. [13]
По этой же причине наличие пор в цинковом покрытии не имеет существенного значения для процесса коррозии железа. Продукты коррозии цинка, увеличиваясь в объеме, частично препятствуют попаданию влаги в поры покрытия. [14]
Составы, содержащие порошок железа, в большинстве случаев являются химически нестойкими, так как процесс коррозии железа в присутствии влаги протекает весьма быстро. [15]
Страницы: 1 2 3