Процесс - коррозия - сплав
Cтраница 1
Процесс коррозии сплава или загрязненного металла определяется работой микрогальванических пар, в большом количестве возникающих на границе раздела металл - электролит. В результате процессов поляризации анодные участки могут пассивироваться настолько, что они становятся катодами по отношению к прежним катодным участкам. После изменения направления тока восстанавливается прежняя система распределения анодных и катодных участков. Явления поляризации коррозионных гальванических пар, как правило, снижают скорость коррозионных процессов. [1]
Процесс коррозии сплава или загрязненного металла определяется работой микрогальванических пар, в большом количестве возникающих на границе раздела металл - электролит. В результате процессов поляризации анодные участки могут пассивироваться настолько, что они становятся катодами по отношению к прежним катодным участкам. После изменения направления тока восстанавливается прежняя система распределения анодных и катодных участков. [2]
Научное исследование процессов коррозии сплавов было до сих пор весьма скудным, и кажется лучше развивать этот предмет теоретически, исходя из различных случаев, которые кажутся возможными, и разбирая реальные примеры, если только они имеются. [3]
Как известно, процесс коррозии углеродистых сплавов в кислотах определяется наличием и эффективностью работы микропар, анодом которых является твердый раствор a - Fe, а катодом - включения, состоящие главным образом из цементита ( Fe3C) или элементарного графита. Присутствие этих включений в железоуглеродистых сплавах обусловлено ограниченной растворимостью углерода в твердом растворе a - Fe в равновесном состоянии. Их электродный потенциал в коррозионных средах более положителен, чем для феррита. [4]
 |
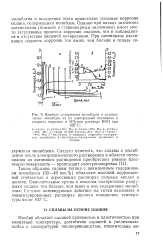
Зависимость коррозионной агрессивности авиационных керосинов от концентрации элементарной серы. [5] |
Исследованиями установлено, что процесс коррозии сплавов меди под влиянием элементарной серы нельзя рассматривать как процесс, протекающий на поверхности металла. Основная масса элементарной серы из топлива проникает в глубь сплава, вступает там во взаимодействие с его компонентами и нарушает его первоначальную структуру. [6]
Переменное смачивание оказывает существенное влияние на процесс коррозии сплавов, в том числе меди и латуни. Во влажном субтропическом климате следует избегать контактов титановых сплавов с углеродистыми сталями и алюминием, так как последние разрушаются. Контакт титановых сплавов с нержавеющими сталями не представляет опасности ввиду малой разности их электродных потенциалов и сильной поляризуемости титановых сплавов. Титановые сплавы более кор-розионностойкие, чем нержавеющие. [7]
От режима термической обработки также зависит инте ность процессов коррозии сплавов Zr с Nb. В этом отноше: предпочтительнее режим, состоящий из закалки и послед го длительного отпуска при 500 С. [8]
Оценивая опасность этого процесса, необходимо учитывать, что по истечении определенного отрезка времени процесс коррозии сплавов циркония будет протекать по линейному закону. Образующаяся при этом белая окисная пленка осыпается с поверхности. [9]
 |
Влияние содержания молибдена в сплавах. [10] |
Однако при низких значениях потенциалов ( близких к стационарным значениям) имеет место затруднение процесса коррозии сплавов, что и наблюдается в отсутствие внешней поляризации. [11]
Недавно произведенное исследование в Германии показало, что размер зерна, как таковой, не является решающим в процессе коррозии сплавов медь-цинк и медь-никель в разбавленной кислоте, хотя механическая и термическая обработка, которая влияет на размер зерна, действует также и на скорость коррозии. [12]
Разработан электрохимический метод определения количеств палладия, рения и меди, накапливающихся на поверхности нержавеющих сталей, и палладия на поверхности титана в процессе коррозии сплавов. [13]
Если перед анодной поляризацией образец титана с 0 01 % Pt был погружен в кипящую 1 % - ную H2S04 в течение нескольких часов, то на кривой в этом случае отсутствует участок активного растворения, сплав ведет себя как пассивный. Было также показано [144], что в процессе коррозии сплава хрома с 0 5 % Pt происходит накопление Pt на поверхности сплава. Об этом свидетельствовало значительное снижение перенапряжения водорода на сплаве после предварительной выдержки образца в коррозионном растворе в течение 45 мин. [14]
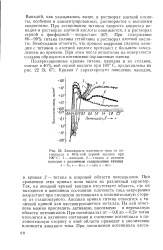 |
Зависимость плотности тока от потенциала в 40 % - ной серной кислоте при 100 С. 1 - ванадия, 2 - титана и сплавов ванадия с различным содержанием титаназ. [15] |
Страницы: 1 2