Процесс - обеззараживание - вода
Cтраница 1
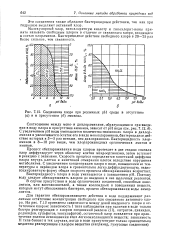 |
Соединения хлора при различных рН среды в отсутствие ( а и в присутствии ( б аммиака. [1] |
Процесс обеззараживания воды хлором протекает в две стадии: сначала хлор диффундирует через оболочку клетки микроорганизма, затем вступает в реакцию с энзимами. Скорость процесса определяется кинетикой диффузии хлора внутрь клетки и кинетикой отмирания клеток вследствие нарушения метаболизма. С увеличением концентрации хлора в воде, повышением ее температуры и переводом хлора в сравнительно легко диффундирующую, недиссоциированную форму общая скорость процесса обеззараживания возрастает. [2]
На процесс обеззараживания воды перекисью водорода большое влияние оказывает микробное заражение воды. [3]
Сущность процесса обеззараживания воды озоном заключается в окислении бактерий атомарным кислородом, образующимся при распаде озона. Озон одновременно уменьшает цветность, запахи и привкусы воды. [4]
Автоматизация процесса обеззараживания воды хлорированием сложна и затруднительна в осуществлении, поэтому хлорирование воды требует сравнительно большого обслуживающего персонала. [5]
В процессе обеззараживания воды гипохлоритом в дозах 5 - 10 мг / л, полученным из смешанных кальциево-натриевых растворов в соотношении 1: 3 с общим солесодержанием 0 427 г-экв / л, в обрабатываемую воду дозируется 1 6 - 3 0 мг-экв / л кальция. [6]
Особенно сильно скорость процесса обеззараживания воды изменяется с температурой в случае применения хлораминов. [7]
Основными факторами, влияющими а процесс обеззараживания воды бактерицидными лучами, являются: а) бактерицидный поток используемых источников излучения; б) поглощение излучения водой; в) сопротивляемость бактерий воздействию бактерицидных лучей. [8]
Основными факторами, влияющими на процесс обеззараживания воды бактерицидными лучами, являются: а) бактерицидный поток используемых источников излучения; б) поглощение излучения водой; в) сопротивляемость бактерий воздействию бактерицидных лучей. [9]
В литературе отмечено отрицательное действие карбаматов на процесс обеззараживания воды с помощью активного хлора. Соединения этого класса, вступая во взаимодействие с хлором, оказывают значительное влияние на хлоропоглощаемость воды, понижая концентрацию остаточного хлора. Наибольшей способностью связывать хлор обладают дитио-карбаматы - ТМТД, цирам, цинеб. Несколько менее реакционноспособ-ными по отношению к хлору оказались эптам, тиллам и севин. [10]
Однако наши исследования показали, что влияние микробной нагрузки на процесс обеззараживания воды перекисью водорода и ионами серебра выражено в значительно меньшей степени, чем при обеззараживании воды одной перекисью водорода и одним серебром. При исход-нон заражении водопроводной воды в концентрации Ю4, 10 и Ю6 особ / л полная ее инактивация наступает после получасового контакта с серебром и перекисью водорода ( рио. Снижение исходного заражения до 10 - Ю особ / л позволяет достигнуть полного обеззараживания через 15 - 20 мин. [11]
 |
Схема гипохлоритного электролизера. [12] |
Дальнейшее увеличение концентрации гипохлори-та сопровождается образованием хлоратов, не обладающих бактерицидным действием и являющихся побочными продуктами в процессе обеззараживания воды. При ведении электролиза в указанном режиме выход по току составляет от 70 ( на титан-двуокисномарган. [13]
Оказалось, что введением в воду аммиака можно очень сильно понизить хлоропоглощение и тем самым снизить расход хлора в процессе обеззараживания воды. [15]
Страницы: 1 2 3