Процесс - образование - перекись
Cтраница 2
Тот факт, что в процессе образования перекисей не происходит полного разрыва связей между атомами кислорода, требующего затраты 117 ккал / моль, позволяет понять, почему автоокисление большого количества веществ протекает сравнительно легко. [16]
Интенсифицирует реакцию с кислородом доставка в зону обработки сжатого кислорода, а также увлажненного воздуха. Последнее объясняется тем, что окисление некоторых металлов в присутствии воды приводит к образованию перекиси водорода. Процесс образования перекиси водорода рассматривают как сопряженный процесс окисления металла и водорода. [17]
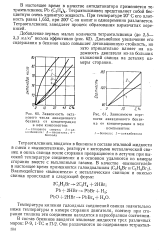 |
Зависимость октанового числа авиационного бензина от концентрации в нем компонентов.| Зависимости сортности авиационного бензина от концентрации в нем компонентов. [18] |
Тетраэтилсвинец представляет собой бесцветную очень ядовитую жидкость. При температуре 20 С его плотность равна 1 652, при 200 С он кипит и одновременно разлагается. Тетраэтилсвинец замедляет процесс образования взрывчатых перекисей. [19]
Дестилляция перекиси содорода из персульфата калии и серной кислоты протекает совершенно гладко, если персульфат смочить разбавленной серной кислотой так, чтобы лишь на поверхности кристаллической массы образовалась кашица, и затем пропускать над этой массой или через нее водяной пар. Этот способ является наиболее удачным решением проблемы выделения перекиси водорода и в таком виде применяется в промышленном масштабе. Так как в процессе образования перекиси водорода внешний обогрев жидкости отсутствует, то дсстилляцию можно производить Б керамиковой реторте. Перекись водорода, полученная по способу Питча и Адольфа, отличается исключительной чистотой, и растворы Н2О2 почти не содержат кислоты н твердого остатка. [20]
Активизированные молекулы кислорода присоединяются к молекулам топлива, образуя так называемые перекиси. Перекиси являются чрезвычайно неустойчивыми соединениями и распадаются при дальнейшем повышении температуры со взрывом, выделяя тепло и воспламеняя остальную массу смеси. Чем интенсивнее будет идти процесс образования перекисей, тем быстрее нормальное горение может перейти в детонационное. [21]
Обезвоженный же перборат, напротив, весьма стоек п й хранении в таблетках. Вследствие малой растворимости пербората гидролиз его водой с образованием перекиси водорода протекает очень медленно при комнатной тем. Поэтому иногда для ускорения процесса образования перекиси в негр добавляют твердые кислоты или вещества, имеющие кислую реакцию. В то время как смесь твердого пербората, содержащего 3 молекулы кристаллизационной воды, с твердыми порошкообразными кислотами разлагается, несколько расплываясь уже При смешении, пербор ат, содержащий 1 - 2 молекулы воды, легко поддается полному смешению с половиной молекулы свободной органической кислоты - винной или лимонной. Если к этой смеси добавить катализаторы - соединения железа, марганца, кобальта или меди, - то при смачивании водой выделяется не перекись водорода, а кислород. Точно так же дезинфицирующие или вяжущие вещества, например, - салициловая кислота или соли таннина или другие соли - алюминия, магния, серебра, висмута или цинка - можно, не опасаясь разложения, смешивать с частично обезвоженным перборатом. [22]
Оно идет нормальным путем и приводит к гидроперекиси и гидроксильным продуктам разложения. Именно это является источником трудностей при использовании металлических редукторов при объемных определениях железа, ванадия и других металлов. В отличие от этого, чистые поверхности меди, железа и других металлов могут служить ингибиторами процессов образования перекисей в избытке эфира. Таким образом, действие металлов при автоокислении может заключаться и в промотировании и в обрыве цепей. Такой двойственный характер, очевидно, можно объяснить электрохимическими свойствами металлических поверхностей. [23]
В том случае, когда перекись водорода используется для консервирования пищевых продуктов, она может оказывать двоякого рода действие: разрушать ферменты, обусловливающие нежелательнее изменение состава, и предотвращать или тормозить рост патогенных или вредных организмов. В связи с тем, что чувствительность, состав и характер обработки и хранения могут колебаться в очень широких пределах ( притом даже при разных пробах одного и того же пищевого продукта или напитка), трудно сделать окончательный вывод о возможной эффективности обработки, об изменении вкуса, питательной ценности или физиологических последствий, которых можно ожидать в каждом отдельном случае в результате обработки перекисью водорода. Ответ на этот вопрос трудно дать еще и потому, что иногда в качестве причины порчи пищепродук-тов выдвигается процесс образования перекиси водорода за счет реакций самоокисления. [24]
В процессе ингибирования происходит образование промежуточных соединений. При исследовании ингибированного 2 6-дибутил-п - крезолом окисления тетралина под действием у-излучения 60СО Вер дин [117] установил, что введение ингибитора не приводит к полному торможению процесса образования перекисей, а только к некоторому его снижению. При радиационном окислении диизопро-пилового эфира установлено [118], что снижение выхода перекисей происходит до значения, соответствующего условиям низкотемпературного окисления. [25]
По-видимому, особо важную роль играют добавки соединений, образующихся в качестве промежуточных продуктов реакции, таких как формальдегид и ацетальдегид. В противоположность этому наблюдения над влиянием аце-тальдегида на смесь 1С5Н12 20а при температуре 329 С и давлении 200 мм рт. ст. ( по-видимому, в период т) показали, что индукционный период после добавления ацетальдегида уменьшается. Однако следует отметить, что в указанных опытах индукционный период не уменьшался до нуля даже при добавлении 5 % ацетальдегида, хотя по данным экспериментаторов [1] это соответствовало приблизительно концентрации ацетальдегида к концу индукционного периода в тех случаях, когда ацетальдегид вообще не добавлялся к смеси. Поэтому Айвазов и Нейман пришли к заключению, что один ацетальдегид не может бьпь причиной мгновенного образования холодного пламени, и предположили, что перекиси, обнаруженные ими в сравнимых количествах, также должны играть известную роль в механизме возникновения холодного пламени. По-видимому, это предположение справедливо, однако возникает вопрос, идентичны ли перекиси, выделяемые из реакционной смеси, тем активным перекисям, которые обусловливают реакцию разветвления цепи в период гг. Вероятно, следует различать, по крайней мере, два процесса образования перекисей. [26]
Страницы: 1 2