Процесс - окисление - метан
Cтраница 2
Экспериментальное определение кинетических параметров процесса окисления метана при температурах выше 1300 К в настоящее время часто осуществляется в ударных трубах. [16]
Из приведенных данных следует, что процесс окисления метана сначала требует значительной энергии активации, но затем протекает с нарастающим термическим эффектом, поэтому реакцию нельзя остановить на промежуточных стадиях. [17]
В более поздних и современных исследованиях процесса окисления метана значительное внимание уделяется изысканию оптимальных условий получения промежуточных продуктов окисления. [18]
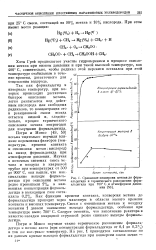 |
Сравнение конверсии метана до формальдегида и термического разложения формальдегида при 700 С и атмосферном давлении. [19] |
Хотя Грей предполагает участие гидроперекиси в процессе окисления метана при низком давлении и при такой высокой температуре, как 400 С, сомнительно, чтобы радикал этой перекиси оставался при этой температуре стабильным в течение времени, достаточного для отщепления водорода. [20]
Принятая в настоящей работе ] химическая модель процесса окисления метана ( табл. 2) основана на предложенной Н. Н. Семеновым радикально-цепной схеме процесса окисления метана. В этой же таблице приведены значения соответствующих констант скоростей реакции. Большинство приведенных значений констант определено в температурном интервале, не превышающем - - - 1000 К; для всех рекомбинацион-ных обрывов приняты обычные значения. [21]
Однако, такого инициирования оказывается недостаточно для осуществления процесса окисления метана с высокой избирательностью по какому-либо продукту неполного окисления. Совместное окисление углеводородов различной реакционной способости приводит к образованию большого набора продуктов с низкой избирательностью по каждому из них. В связи с чем большого практического значения эти процессы не имеют. [22]
Однако, такого инициирования оказывается недостаточно для осуществления процесса окисления метана с высокой избирательностью, по какому-либо продукту неполного окисления. Совместное окисление углеводородов различной реакционной способости приводит к образованию большого набора продуктов с низкой избирательностью по каждому из них. В связи с чем большого практического значения эти процессы не имеют. [23]
Сколько-нибудь существенное каталитическое действие стенок реакционного канала как на процесс окисления метана, так и на образование ацетилена, весьма сомнительно. [24]
Отметим, что Фурман и Шестакова [62], изучив процесс окисления метана ( лишенного примесей высших гомологов) под давлением, определили влияние на характер процесса давления, температуры, концентрации кислорода, времени пребывания исходной смеси и продуктов реакции в реакционной зоне. [25]
В табл. 16 приведены численные значения суммарной энергии активации процесса окисления метана, полученные различными исследователями. Анализ данных таблицы показывает, что численные значения энергии активации процесса окисления метана в интервале 500 - 1500 К, определяемые в статических и динамических условиях колеблются от 40 до 80 ккал / моль, при температурах выше 1500 численные значения энергии активации, определяемые в ударных волнах, лежат в интервале 20 - 50 ккал / моль. [26]
Надо иметь в виду, что вся совокупность физико-химических условий протекания процесса окисления метана чрезвычайно неблагоприятна для стабилизации образовавшегося формальдегида. [27]
Большое количество экспериментальных работ проведено для подтверждения определяющей роли формальдегида в процессе окисления метана. [28]
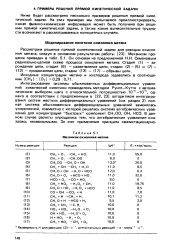 |
Механизм окисления метана. [29] |
Механизм процесса приведен в табл. 5.1. Он основан на предложенной Н.Н. Семеновым радикально-цепной схеме процесса окисления метана. Стадия ( 1) - зарождение цепи, стадия ( 6) - разветвление цепи, стадии ( 2) - ( 5) и ( 7) - ( 12) - продолжение цепи, стадии ( 13) - ( 17) - обрывы цепи. [30]
Страницы: 1 2 3 4