Процесс - окисление - метанол
Cтраница 1
Процесс окисления метанола ведется при давлении 0 6 кгс / сж2 и температуре 620 - 650 С. [1]
Процесс окисления метанола осуществляется в вертикальных реакторах ( контактных аппаратах), внутри которых на решетках размещен катализатор. Перегретые пары метанола подаются сверху. Для отнятия теплоты экзотермической реакции в реакторе имеется внутренний трубчатый холодильник, охлаждаемый водой. [2]
 |
Контактный аппарат для окисления метанола. [3] |
Процесс окисления метанола осуществляется в вертикальных реакторах ( контактных аппаратах), внутри которых на решетках размещен катализатор. Перегретые пары метанола подаются сверху. Для отнятия теплоты экзотермической реакции в реакторе имеется внутренний трубчатый холодильник, охлаждаемый водой. Слой катализатора 4 ( в виде кристаллов размером 2 - 3 мм) высотой 20 мм помещен на посеребренной медной сетке, поддерживаемой решеткой. Вход перегретой метаноло-воздушной смеси осуществляется непрерывно сверху. Продукты реакции окисления удаляются снизу. [4]
Процесс окисления метанола в формальдегид может протекать и на окис-ных катализаторах. Окисные катализаторы по сравнению с металлическими имеют как преимущества, так и недостатки. Процесс на ряде окислов металлов ведется при более низких температурах ( 300 - 350), и идет он со значительно меньшим выходом побочных продуктов, однако на окисление одновременно требуется 8 - 10-кратный избыток кислорода. [5]
Для процесса окисления метанола в формальдегид на железо-молибденовом катализаторе, осуществляемого в комбинированном реакторе, наиболее опасны для трубчатой части аппарата неоднородности температуры хладоагента и активности катализатора, а для адиабатического слоя - неоднородности содержания непрореагировавшего метанола на входе и константы скорости окисления формальдегида. Для процесса окисления двуокиси серы наиболее опасна неоднородность по начальной температуре перед слоем, так как ее вредное влияние часто не может быть устранено никаким запасом катализатора. [6]
Переход от процесса окисления метанола к разряду аниона моноэфира наблюдается на золотом, родиевом и иридиевом электродах при плотностях тока соответственно в 15 - 20, 6 - 7 и 3 - 4 раза больших, чем на платиновом аноде, что предопределяет меньший выход продукта по току на этих электродах. [7]
Влияние давления на процесс окисления метанола иллюстрируется данными таблицы. Изменение давления от 50 до 100 ат приводит к увеличению скорости процесса, что выражается в увеличении превращения реагирующих веществ - метанола и кислорода, и некоторому повышению концентрации полезных продуктов. Наблюдаемое ускорение процесса, по-видимому, связано с ростом концентрации кислорода в зоне реакции при увеличении давления. [8]
Воздух, идущий для процесса окисления метанола, должен быть совершенно1 чистым и не содержать в себе механических примесей. Вода, требующаяся для абсорбции формальдегида и для разбавления его до требуемой концентрации, не должна содержать солей железа, алюминия, а также органических веществ. [9]
Большая чувствительность температуры в процессе окисления метанола объясняет более сильное влияние неравномерного профиля скорости. [10]
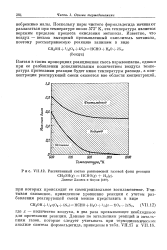 |
Рассчитанный состав равновесной газовой фазы реакции. [11] |
Поскольку пары чистого формальдегида начинают разлагаться при температуре около 573 К, эта температура является верхним пределом процесса окисления метанола. [12]
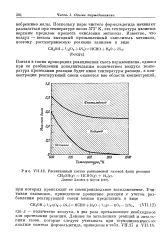 |
Рассчитанный состав равновесной газовой фазы реакции. [13] |
Поскольку пары чистого формальдегида начинают разлагаться при температуре около 573 К, эта температура является верхним пределом процесса окисления метанола. [14]
Сравнение кривых электроокисления веществ, хемосорби-рующихся при поляризации электродов из платины и э.с.о. ( Pt: Ru 9: 1), показывает, что наблюдаются заметные различия в потенциалах начала окисления, характере окисления и потенциалах полного окисления хемосорбирующихся веществ на этих электродах. Кривые электроокисления на э.с.о. в кислом и щелочном растворах близки друг к другу. Перенапряжения окисления хемосорбированного вещества и процесса окисления метанола в стационарных условиях на э.с.о. в растворе различаются на - 25 мв. [15]
Страницы: 1 2