Процесс - окисление - окись - углерод
Cтраница 2
Наиболее важным вопросом механизма реакции углерода с кислородом является вопрос о первичных продуктах реакции: является ли двуокись углерода первичным продуктом реакции углерода с кислородом или она вторичный продукт, образующийся при окислении в газовой фазе окиси углерода. Правильное экспериментальное решение этого вопроса затрудняется наличием процесса окисления окиси углерода в газовой фазе. [16]
Являясь продуктом неполного окисления, окись углерода сама представляет собой горючий газ, способный к дальнейшему окислению. На основании молекулярных весов можно составить материальный баланс процесса окисления окиси углерода: на 28 кг ее требуется 16 кг кислорода; в результате реакции образуется 28 16 44 кг двуокиси углерода. Пересчет на объемные единицы показывает, что на 1 м3 окиси углерода при нормальных условиях затрачивается 0 5 м3 кислорода. При этом образуется 1 м3 двуокиси углерода с выделением 3020 ккал. [17]
В доставленном нами исследовании были учтены недостатки работы Лэмба и Вейля. Количество катализатора было подобрано таким образом, что эффективность процесса окисления окиси углерода не достигала 100 % даже ( В отсутствие влаги. В качестве меры активности катализатора было принято количество окиси углерода, окисленное в углекислоту и выраженное в процентах от ее исходной концентрации. При постоянном значении исходной концентрации эта величина пропорциональна константе скорости реакции нулевого порядка. Специальная экспериментальная проверка показала, что количество окисленной окиси углерода пропорционально высоте слоя катализатора, что соответствует нулевому порядку реакции по отношению к окиси углерода. [19]
В то же время добавка ионов трехвалентного хрома снижает проводимость и увеличивает энергию активации каталитической реакции. Эти наблюдения согласуются с заключениями о том, что скорость процесса окисления окиси углерода определяется стадией образования положительных ионов на поверхности окисла никеля - полупроводника р-типа. [20]
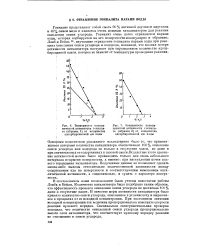
Эта же реакция разложения на окислах n - типа ( например, на ZnO) сопровождается уменьшением электропроводности катализатора. Кроме того, Бейкер и Дженкинс указали, что результаты опытов по введению в окислы добавок ( см. разд. Теперь обратимся к сопоставлению каталитической активности полупроводниковых окислов в процессе окисления окиси углерода. Шваб [ 97 показал, что характер дефектов ( электронные свойства) окислов металлов, играет доминирующую роль в каталитическом действии этих твердых тел. Как было объяснено ранее в этой главе, Вервей [26, 27] показал, что добавление одновалентных катионов, таких, как литий, к матрице из окисла никеля дает в результате увеличение числа дырок в этом окисле и, следовательно, повышает проводимость jj - типа. И, наоборот, при добавлении трехвалентных ионов ( таких, как хром) число дырок уменьшается и проводимость, следовательно, снижается. В нижней части рис. 23: Шваб приводит данные Вервея [26] и Хауффе [98], иллюстрирующие влияние добавленных ионов на проводимость закиси никеля. В верхней части рисунка приведены данные, полученные для реакции каталитического окисления окиси углерода. [21]
Вопрос о первичных продуктах реакции - основной в механизме этой реакции. Были выдвинуты различные теории, объясняющие, какие продукты реакции горения у лерода являются первичными. Правильное экспериментальное решение вопроса о первичных продуктах реакции горения затрудняется наличием процессов окисления окиси углерода в газовой фазе и восстановления двуокиси углерода. [22]
Окись углерода образуется как промежуточный продукт химической реакции углеродсодержащего топлива с кислородом. При подаче недостаточного количества кислорода, как это имеет место в богатых смесях, окись углерода является конечным продуктом горения. В бедных смесях окись углерода может образоваться по одной из следующих двух причин. Во-первых, существует возможность неполного смешения топлива с воздухом в реакционной зоне, так что отдельные участки этой зоны работают на богатых смесях, несмотря на общий избыток кислорода во всей смеси. Во-вторых, окись углерода может образоваться в высокотемпературных точках зоны горения, где химическое равновесие смещено в сторону диссоциации двуокиси углерода. В табл. 6.7 для разных температур приведены значения константы равновесия идеальных газов Кр, которое устанавливается в процессе окисления окиси углерода до двуокиси углерода. [23]
Страницы: 1 2