Процесс - отрыв - атом - водород
Cтраница 1
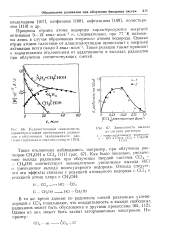 |
Количественные зависимости, характеризующие превращения радикалов в облученном замороженном рас-ткоре гидразина в этиловом спирте 1103 ].| Зависимость выхода. [1] |
Процессы отрыва атома водорода характеризуются энергией активации 9 - 12 ккал-моль 1 и, следовательно, при 77 К возможны лишь в случае образования горячих атомов водорода. Такие реакции также приводят к значительным отклонениям от аддитивности в выходах радикалов при облучении соответствующих смесей. [2]
Тем не менее процесс внешнего отрыва атома водорода гораздо медленнее процесса внутреннего отрыва атома водорода; поэтому механизм не может объяснить эффективный процесс разветвления цепи и, следовательно, процесс самовоспламенения. [4]
Учет энергетических факторов является существенным при рассмотрении процессов отрыва атома водорода. Это вытекает из следующих наблюдений: в алканах ионы, образовавшиеся в результате отрыва нечетного числа атомов водорода от молекулярного иона, составляют большую часть по сравнению с ионами, получающимися после отрыва четного числа водородных атомов. Однако для ароматических систем наблюдается вполне определенная тенденция к снижению интенсивности тех ионов, для образования которых необходимо оторвать от молекулярного иона большее число атомов водорода. [5]
Тем не менее процесс внешнего отрыва атома водорода гораздо медленнее процесса внутреннего отрыва атома водорода; поэтому механизм не может объяснить эффективный процесс разветвления цепи и, следовательно, процесс самовоспламенения. [6]
Энергия связи С - Н 3 7 эв и, вероятно, энергия активации процесса отрыва атома водорода составляет около 2 эв, что соответствует лишь 5 - 6 % всей энергии, поглощаемой при образовании пары ионов. Поэтому образующиеся полимерные радикалы должны находиться в состоянии высокого возбуждения. [7]
Дж / мдль) [4]; то легко понять, почему замещение у атома углерода протекает несравнимо более медленно, чем процесс отрыва атома водорода. [8]
Дж / моль) [4], то легко понять, почему замещение у атома углерода протекает несравнимо более медленно, чем процесс отрыва атома водорода. [9]
В указанном ряду происходит увеличение устойчивости свободных радикалов, что видно из рассмотрения данных по энергиям диссоциации связей С - Н в соответствующих углеводородах. Это приводит к уменьшению экзотермичности процесса отрыва атома водорода от растворителя и, по правилу Поляни - Семенова, к увеличению энергии активации процесса и, следовательно, к уменьшению его скорости. В то же время скорость рекомбинации радикалов повышается, поскольку увеличивается время жизни свободных радикалов и, следовательно, их концентрация. Таким образом, отношение Ra / RH должно возрастать при переходе от метила к бензилу. [10]
Анализ данных по энергии связи между различными атомами углерода Г I.5 J наводит на мысль об образовании фенантрилметиленовых моно-дн-и трирадика-лов в продуктах деструкции моно -, ди-и триоктилфенантрвнов. Учитывая то, что образование фенантрилметиленовых радикалов идет в конденсированной системе, с большой вероятностью можно предсказать протекание процессов отрыва атомов водорода этими радикалами от соседних углеводородных молекул. [11]
Образующиеся ион-радикалы стабилизируются в ионной решетке. Так как в спектрах у-облученного хлорида гидразония фиксируется атомарный водород и не отмечается изменения концентрации ион-радикалов при гибели Н, то процессы N2H T Н - - N2H4 Н2 или N2H4 Н - - N2H3, по-видимому, сравнительно маловероятны. Сопоставление этих данных с данными об образовании парамагнитных частиц при облучении солей, анионы которых также содержат водород, показывает, что процессы отрыва атома водорода имеют достаточно большую вероятность и происходят как в катионах, так и в анионах. [12]
Состояние п, л рассматривают как резонансный гибрид двух структур с возбужденным электроном на р -: - орбитали кислорода и на / - орбитали углерода. Кроме повышения общей электронной плотности л-системы в возбужденном состоянии в результате добавления одного / 7у - электрона, наблюдается также уменьшение или обращение поляризации С О-группы, характерной для основного состояния вследствие наличия в одной из резонансных структур положительного заряда на кислороде и отрицательного заряда на углероде. Электронный дефицит на кислородном атоме после удаления n - электрона приводит к возникновению электрофильного центра на карбонильном атоме кислорода [367-369], который, кроме этого, имеет характер свободного радикала [347, 370] благодаря незначительному перекрыванию / г-орбитали с другими молекулярными орбиталями. Поэтому п, л - состояние карбонильных производных обладает высокой реакционной способностью в процессах отрыва атома водорода или электрона от других соединений. [13]
На стеклах, имеющих различную предварительную обработку, вреыя жизни р - бензохиьона различно, кривые ( а) и ( с) рмс. Данные, представленные кривой ( а), были получены для стекол, откачанных при 200 С. Данные, представленные кривой ( с), были получены для етенла, обработанного в 2.0 при 300 С в течение I часа и откачанного при 200 С. Следовательно, наблюдается изотопный эффект для химического процесса. Этот факт приводит нас к заключению, что процесс, зависимый от температуры, константа скорости которого дается выражением ( 7), есть процесс отрыва атома водорода от поверхностных гидроксильных групп р - бен-зохиноном в триплетном сосгоянш. Этот вывод разумен и в связи с тем, что пТТ триплетное состояние карбонильных соединений отрывает атом водорода от различных соединений. [14]
Страницы: 1
