Процесс - производство - хлор
Cтраница 1
 |
Электролизер фирмы Окситек. [1] |
Процесс производства хлора и гидроксида натрия по мембранному методу, а также элементы конструкции мембранных электролизеров непрерывно совершенствуется. В недалеком будущем ожидается появление новых ионообменных мембраны и конструкций электролизеров, которые позволят получить раствор гидроксида натрия с концентрацией 46 - 50 % непосредственно в электролизере и существенно сократить энергетические затраты на производство гидроксида натрия. [2]
В процессе производства хлора и каустической соды электролизом водных растворов хлоридов щелочных металлов выделяется водород, при производстве по методу электролиза с ртутным катодом водород загрязнен парами ртути. При диафрагменном методе производства водород не содержит ртути, но может включать помимо примесей кислорода и азота также небольшие количества хлорор-ганических продуктов, образующихся в анодном пространстве электролизера и поступающих затем в катодное пространство вместе с потоком анолита. [3]
Существуют три разновидности процесса производства хлора: а) ртут - 1ЫЙ метод, б) диафрагменный метод и в) мембранный метод. Первые два метода были разработаны в 1880 - х годах, третий - в 1960 - х годах. Во всех случаях на аноде электролитически выделяется хлор чз счет разряда хлорид-ионов. В ртутном методе применяют ртутный катод. [4]
Водород является побочным продуктом процесса производства хлора методом электролиза соляных растворов. В определенной концентрации хлор образует горючие и взрывчатые смеси с водородом, а его реакции с некоторыми органическими соединениями, например углеводородами, спиртами и простыми эфирами, могут иметь взрывной экзотермический характер, если не контролируются соответствующим образом. Реакция хлора с водородом может начаться под воздействием прямых солнечных лучей и иных источников ультрафиолетового излучения, статического электричества или резкого удара. [5]
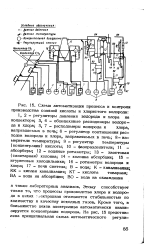 |
Схема автоматизации процесса и контроля производства соляной кислоты и хлористого водорода. [6] |
Этому способствует также то, что процессы производства хлора и водорода в цехах лектролиза отличаются стабильностью по количеству и качеству исходных газов. Кроме того, в большинстве цехов электролиза автоматически анализируется концентрация водорода. [7]
Небольшие количества трихлорида азота, которые могут образоваться в процессе производства хлора, очень неустойчивы и обладают высокой взрывоопасностью. При испарении хлора, содержащего небольшое количество трихлорида азота, концентрация трихлорида азота может достичь опасной величины в оставшемся жидком хлоре. [8]
Описанный процесс позволяет проводить одновременную переработку всех твердых и жидких отходов, образующихся в процессе производства хлора в ртутном электролизере. [9]
Перечисленные выше обстоятельства привели к тому, что нагрузка на электролизеры с монополярным включением электродов во многих процессах промышленной электрохимии за последние 10 - 15 лет значительно выросла. Тенденция к дальнейшему повышению нагрузки на электролизер ясно видна в процессах производства хлора, а также при получении хлоратов, перекиси водорода, перхлоратов, соединений марганца и других продуктов. [10]
Поворотные заслонки ( поворотные затворы) в отечественной хлорной промышленности применяют крайне редко. Из отечественных конструкций используют в качестве запорных органов титановые заслонки типа 32тн614п, имеющие седло из фторопласта-4. Эти поворотные заслонки используют на коммуникациях влажного хлора в процессах производства хлора. [11]
Кррме манганитов двухвалентного марганца известен ряд других манта - витое. Некоторые из иих играют очень важную роль в аналитической химии, как, например, биманганиты цинка и кальция. Биманганит кальция имеет техническое значение, являясь промежуточным продуктом при регенерации марганца в вельдоновском процессе производства хлора. [12]
Кррме манганитов двухвалентного марганца известен ряд других маяга-нитов. Некоторые из них играют очень важную роль в аналитической химии, как, например, биманганиты цинка и кальция. Биманганит кальция имеет техническое значение, являясь промежуточным продуктом при регенерации марганца в вельдонов ском процессе производства хлора. [13]
В производстве хлора и каустической соды для предотвращения проникновения хлора в атмосферу цеха вся аппаратура и трубопроводы должны быть герметизированы. При содержании в водороде более 4 масс. % хлора возникает взрывоопасная смесь, поэтому вакуум в катодном пространстве электролизера должен быть выше вакуума в анодном пространстве. При электролизе с ртутным катодом особую опасность для обслуживающего персонала и для окружающей среды представляет ртуть. Для уменьшения потерь ртути процесс производства хлора и щелочи осуществляют по замкнутой технологической схеме, которая предусматривает возвращение загрязненных ртутью конденсатов и вод обратно в процесс. [14]
Зная лишь о том, что завозится на фабрику и что вывозится из нее, и не подозревая о существовании промежуточных стадий, мы объявили бы соединения марганца катализаторами. Они ведь в самом деле не расходуются, если не считать неизбежных случайных потерь. Между тем из второго уравнения явствует, что решающую роль в способе Вельдона, как и в способе Шееле, играет именно соединение четырехвалентного марганца СаМпОз. В процессе своего образования оно присоединяет кислород, а затем в процессе взаимодействия с хлористым водородом отщепляет его вновь, окисляя НС1 в СЬ - Совместить оба процесса во времени в пространстве нельзя, так как они протекают при взаимоисключающих условиях: для окисления марганца требуется щелочная среда, созданию которой служит обработка известью, а для обратного восстановления требуется кислая среда. Поэтому процесс производства хлора по способу Вельдона неизбежно1 является циклическим, и превращение его в непрерывный процесс принципиально невозможно. [15]
Страницы: 1 2