Процесс - распад - бикарбонат
Cтраница 1
Процесс распада бикарбонатов протекает тем быстрее, чем выше температура и чем энергичнее перемешивание. В прямоточных системах распад бикарбонатов обусловлен нагреванием воды, а в оборотных системах, кроме того, потерей растворенной в воде углекислоты при разбрызгивании воды на градирнях или брызгаль-ных бассейнах. [1]
Процесс распада бикарбонатов протекает тем быстрее, чем выше температура и чем энергичнее перемешивание. В прямоточных системах охлаждения распад бикарбонатов обусловлен нагреванием воды, а в оборотных системах, кроме того, потерей растворенной в воде углекислоты при разбрызгивании воды в градирнях или брызгальных бассейнах. [2]
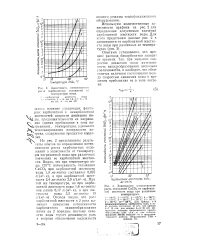 |
Зависимость интенсивности роста отложений СаС03 от карбонатной жесткости воды при различных температурах. [3] |
Опытами установлено, что процесс распада бикарбонатов зависит от времени. [4]
В связи с этим представляет большой интерес количественная оценка процессов распада бикарбоната кальция и образования карбонатных отложений при нарушении углекислотного равновесия в системах оборотного водоснабжения, а также определение дозы углекислоты, необходимой для предотвращения этих процессов. [5]
По мере увеличения скорости протекания воды в холодильнике интенсивность процесса распада бикарбоната кальция уменьшается. [6]
В связи с нагревом в залежи закачиваемой воды в поровом пространстве может протекать процесс распада бикарбонатов и образования осадка карбоната кальция. [7]
Поэтому основная задача сводится к нахождению опытных зависимостей интенсивности накипеобразования от ряда факторов, влияющих на процесс распада бикарбонатов и на процесс отложений карбонатов на поверхностях нагрева в условиях работы теплофикационного оборудования. [8]
Присутствие в оборотной воде ионов С1 - и SO - , связанных с ионом Са2, ускоряет процесс распада бикарбоната кальция и в известной степени интенсифицирует выпадение карбоната кальция; присутствие в воде тех же ионов, связанных с ионами Mg2 и Na, на процесс распада бикарбоната кальция отрицательно не влияет; наоборот, отмечается, что магниевые соли в; оборотной воде придают даже некоторую стойкость бикарбонату кальция. [9]
Присутствие в оборотной воде ионов С1 - и SO - , связанных с ионом Са2, ускоряет процесс распада бикарбоната кальция и в известной степени интенсифицирует выпадение карбоната кальция; присутствие в воде тех же ионов, связанных с ионами Mg2 и Na, на процесс распада бикарбоната кальция отрицательно не влияет; наоборот, отмечается, что магниевые соли в; оборотной воде придают даже некоторую стойкость бикарбонату кальция. [10]
Коэффициент концентрирования бикарбонатов из-за частичного распада этих солей при отсутствии обработки воды обычно значительно меньше коэффициента концентрирования не выпадающих в осадок солей. Расхождение между этими двумя коэффициентами определяется интенсивностью процесса распада бикарбоната кальция. [11]
Особый интерес представляет подготовка воды для систем охлаждения. Магнитная обработка повышает структурную температуру и тем самым ускоряет процесс распада бикарбонатов и выделения накипеобразо-вателей. Однако если без обработки воды распад бикарбонатов и пересыщение, наблюдающееся у поверхностей нагрева, сопровождаются выделением накипеобразовате-лей, цементирующих оттесняемые к стенкам при движении жидкости взвешенные глинистые и другие частицы, то выделение накипеобразователей в объеме жидкости в результате воздействия на воду магнитных полей исключает этот процесс. [12]
Вместе с тем воздушноводяное соотношение должно быть адекватно содержанию железа в обрабатываемой воде. Это объясняется тем, что в процессе аэрации удаляется не только свободная углекислота, содержащаяся в исходной воде, но и углекислота, образующаяся в процессе распада бикарбонатов. [13]
В тех случаях, когда этот способ не дает улучшения или приводит к чрезмерному перерасходованию средств на подачу дополнительного количества - воды, могут быть применены описываемые ниже методы обработки воды - подкис ление, рекарбонизация, фосфатирование. Дозы кислоты или оксида углерода подбираются для каждой действующей прямоточной системы экспериментальным путем с тем, чтобы в теплообменных аппаратах и трубах оставался тонкий слой накипи, предохраняющий металл от коррозии. В связи с кратковременностью пребывания воды в аппаратах и трубопроводах прямоточных систем охлаждения, достаточны дозы кислоты или оксида углерода, составляющие лишь часть соответствующих доз, необходимых для полной стабилизации воды. При добавлении в воду этих дефицитных доз процесс распада бикарбонатов должен замедляться в такой степени, чтобы он не проходил за небольшое время пребывания воды в прямоточной системе. [14]
Страницы: 1