Процесс - распад - гидроперекись
Cтраница 1
Процесс распада гидроперекисей в присутствии гетерогенного катализатора е всегда, однако, осуществляется по такому механизму. [1]
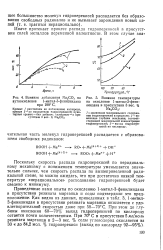 |
Влияние добавления Na2CO3 на.| Влияние температуры на окисление 1-метил - З - фенилиндана в присутствии 3 вес. % Na2CO3. [2] |
Иначе протекает процесс распада гидроперекисей в присутствии солей металлов переменной валентности. [3]
При завышении температуры в колонне окисления возможен процесс распада гидроперекиси изопропилбензола со взрывом. Для предотвращения этого должны быть предусмотрены блокировки: прекращающие подачу технологического воздуха в систему ( закрывается отсечной клапан на линии подачи технологического воздуха); включающие подачу умягченной воды в случае остановки насоса, подающего химически очищенную воду в колонну окисления. При отсутствии умягченной воды должна иметься возможность подачи промышленной воды с другого водовода. В случае термического распада гидроперекиси в колоннах окисления должна открыться электрозадвижка, управляемая со щита контрольно-измерительных приборов, и содержимое аппарата должно сливаться в аварийную емкость. [4]
Таким образом, спектрофотометрические измерения количественно подтверждают вывод об изменении валентного состояния катализатора в процессе катализированного распада гидроперекиси. [5]
Это приводит к увеличению скорости образования свободных радикалов. Процесс распада промежуточных гидроперекисей на рндикалы представляет собой реакцию вырожденного разветвления цепей. [6]
В процессе автоокисления гидроперекись по реакции ( 3) распадается на радикалы, что приводит к увеличению скорости образования свободных радикалов. Процесс распада промежуточных гидроперекисей на радикалы представляет собой реакцию вырожденного разветвления цепей. [7]
Однако предварительный расчет изменения значений концентраций гидроперекиси во времени по уравнению, соответствующему схеме реакций ( 1) и ( 2), показал, что почти во всех случаях катализа расчетные кривые оказываются ниже экспериментально найденных значений концентраций. Данный факт указывает на наличие торможения в процессе распада гидроперекиси. [8]
Однако предварительный расчет изменения значений концентраций гидроперекиси во времени но уравнению, соответствующему схеме реакций ( 1) и ( 2), показал, что почти во всех случаях катализа расчетные кривые оказываются ниже экспериментально найденных значений концентраций. Данный факт указывает на наличие торможения в процессе распада гидроперекиси. [9]
Оба рассмотренных класса ингибиторов предназначаются для стабилизации полипропилена против термоокислительной деструкции. При температурах выше 160 С хорошим стабилизирующим действием обладают лишь ингибиторы первого класса или-смеси ингибиторов первого и второго классов; ингибиторы же второго класса в чистом виде надежны только при более низких температурах. Это связано со скоростью образования радикалов в процессе распада гидроперекисей при различных температурах. В условиях низкой температуры гидроперекиси распадаются относительно медленно. Высокая концентрация радикалов появляется в полимере лишь после накопления гидроперекисей. Если в полимере присутствует вещество, которое эффективно снижает концентрацию гидроперекисей, скорость термоокислительной деструкции резко уменьшается. При повышенных температурах гидроперекиси распадаются очень быстро, их стационарная концентрация при значительной концентрации радикалов относительно невысока. Таким образом, напрашивается вывод, что хорошим стабилизирующим эффектом обладают лишь такие вещества, которые, реагируя с радикалами, дают малоактивные продукты. [10]
На процесс окисления изопропилбензола большое влияние оказывает рН среды. Скорость окисления в кислой среде ( рН 6) значительно снижается, а в щелочной среде ( рН 7 5) возрастает. Это связано с необходимостью нейтрализации кислых продуктов, содержа-цдехся в сырье и образующихся в процессе распада гидроперекиси, поскольку они ингибируют окисление. Кроме того, щелочь ускоряет инициирование цепей окисления. [11]
Страницы: 1