Процесс - растворение - вещество
Cтраница 3
Наконец, еще одним из важнейших признаков истинных растворов является самопроизвольное образование. В процессе растворения вещества, как отмечалось выше, уменьшаются свободная энергия и изобарно-изотермический потенциал системы. [31]
Так что настало время вспомнить о гипотезах, которые мы при нимали на веру, создавая математическую модель задачи. Например, мы фактически предположили, что процессы растворения участвующих веществ независимы. [32]
Было показано также, что структурное состояние воды оказывает существенное влияние на протекание процессов растворения веществ и гидратации ионов. В связи с этим представляет значительный интерес разработка методов нахождения вкладов в термодинамические функции гидратации, которые бы характеризовали структурные изменения воды в указанных ионных процессах. [33]
 |
Растворимость различных твердых веществ в воде. [34] |
Изменение растворимости с температурой обусловлено влиянием кинетической энергии молекул растворенного вещества и растворителя, а кроме того, определяется устойчивостью сольватированных частиц и энергией кристаллической решетки. Результат одновременного действия всех перечисленных факторов можно предсказать, зная теплоту растворения: если процесс растворения вещества происходит эндотермически, то при повышении температуры его растворимость должна возрастать. [35]
Большое значение для точности анализа имеет также и процесс улавливания продуктов отгона. В том случае, когда отгоняемые вещества улавливаются каким-либо растворителем, следует помнить, что процесс растворения веществ в любом растворителе не протекает мгновенно, и скорость его зависит от ряда причин. В частности, скорость улавливания газо - и парообразных продуктов зависит от растворимости данного вещества в применяемом растворителе, от скорости прохождения газа или пара через поглощающий раствор, от размера пузырьков проходящего через раствор газа, от концентрации улавливаемого вещества в газе-носптеле, от концентрации поглощающей жидкости и высоты поглощающего слоя, от температуры газа и поглощающей жидкости, а для такого растворителя, как вода, также и от рН раствора и его изменения в процессе поглощения отгоняемых веществ. [36]
Вещество засыпают в колбу с растворителем, предварительно нагретым до температуры, на 10 - 20 С выше предполагаемой температуры насыщения. Затем колбу с растворителем и растворяемым веществом выдерживают при этой температуре, с тем чтобы ускорить процесс растворения вещества. Значительного перегрева, тем более вскипания, раствора надо избегать, так как это увеличивает потерю растворителя. Для того чтобы избежать перегрева раствора, колбу при нагревании помещают в водяную баню. [37]
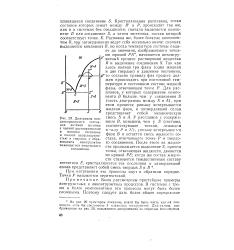 |
Диаграмма кон - смесь S и Л. У расплавов с содержа-денсированного состоя - нием В, меньшим, чем у S ( составы. [38] |
Кристаллизация расплавов, точки составов которых лежат между В и Р, происходит так же, как и в системах без соединения: сначала выделяется компонент В или соединение S, а затем эвтектика, состав которой соответствует точке. Расплавы же, более богатые компонентом В, при затвердевании ведут себя несколько иначе: сначала выделяется компонент В, но когда температура системы падает до значения, изображаемого точка - ( ми прямой РА, начинается инконгру-энтный процесс растворения вещества В и выделение соединения S. [39]
 |
Образование молекул метана ( а, аммиака ( б и воды ( в в результате перекрывания s - орбиталей атомов водорода с 1р3 - гибридными ор-биталями центрального атома. [40] |
Задумались ли вы, почему одни вещества с водой образуют однородную систему, а другие - неоднородную. Чтобы ответить на этот вопрос, следует выяснить, что происходит в процессе растворения веществ в воде. При растворении вещества измельчаются - дробятся. Дисперсных систем известно много. Они различаются между собой в зависимости от того, какие частицы ( твердые, жидкие, газообразные) и в какой среде ( жидкой, газообразной) распределены. Так, например, одной из таких дисперсных систем являются дым или пыль в воздухе: воздух - смесь газов, а частицы - мелкораздробленные твердые вещества. [41]
Подробно исследовались простые реакции соединения между твердыми веществами типа A - fB - АВ, примером которых может служить образование оксисоли или смешанного окисла из двух составляющих его окислов ( см. [2], стр. Способ роста этого слоя зависит от способности А и В диффундировать через массу АВ; в предельном случае, когда А может диффундировать через АВ, а В нет, А будет входить в слой АВ на поверхности раздела А / АВ, диффундировать через него и соединяться с В на поверхности раздела АВ / В. Поэтому слой АВ будет расти на той стороне, где находится В; кажущаяся реакция на стороне слоя, где находится вещество А, в действительности является процессом растворения вещества А, которое, таким образом, входит в слой продукта. В случае, если А и В способны диффундировать в слой АВ, их соединение будет происходить в самом слое, рост которого при этом происходит за счет прогрессивного расходования масс обоих соприкасающихся реагентов. [42]
В-третьих, ионные реакции протекают с необычно высокими скоростями. Часто скорость реакции настолько велика, что ее измерение оказалось возможным лишь с помощью новейших методов. Высокая скорость некоторых реакций, например реакций нейтрализации или осаждения, может быть объяснена только на основе теории электролитической диссоциации исходя из представлений о том, что образование ионов происходит непосредственно в процессе растворения вещества. [43]
Кристаллическая решетка этой соли состоит из ионов Ва и SO4, которые под действием диполей воды будут уходить с поверхности кристаллов в раствор. Ведь двигающиеся в растворе ионы Ва и SO могут сталкиваться с поверхностью кристаллов BaSO4 и осаждаться под влиянием притяжения других ионов. Постепенно скорость процесса растворения вещества уменьшается, а скорость противоположного процесса осаждения увеличивается, что и приводит к состоянию динамического равновесия. [44]
Как правило, при растворении поглощается или выделяется тепло и происходит изменение объема раствора. Объясняется это тем, что при растворении вещества происходит два процесса: разрушение структуры растворяемого вещества и взаимодействие частиц растворителя с частицами растворенного вещества. Оба эти процесса сопровождаются различными изменениями энергии. Для разрушения структуры растворяемого вещества требуется затрата энергии, тогда как при взаимодействии частиц растворителя с частицами растворенного вещества происходит выделение энергии. В зависимости от соотношения этих тепловых эффектов процесс растворения вещества может быть эндотермическим или экзотермическим. Тепловые эффекты при растворении различных веществ различны. При растворении в воде азотно-1 кислого калия или азотнокислого аммония температура раствора резко понижается ( эндотермические процессы), а при растворении в воде хлористого натрия температура раствора практически не меняется. [45]
Страницы: 1 2 3 4