Процесс - рекомбинация - атом
Cтраница 2
Отравляющее действие окислов азота на образование озона можно объяснить их ролью в процессах рекомбинации атомов кислорода. Известно, что окислы азота могут играть роль катализатора в этих процессах. [16]
К ним относятся взаимодействия NO с Н2, С2, СЬ, Вг2, а также процессы рекомбинации атомов или свободных радикалов в молекулы, реакции окисления - восстановления. [17]
Платиновые металлы обладают высокой способностью активировать водород, в соответствии с этим на них легко протекают процессы рекомбинации атомов водорода, о-га-превращения, гомомолекулярный изотопный обмен водорода. [18]
Атомарный водород, выделяющийся в первичном фотохимическом акте, несомненно будет обладать в наших условиях малой подвижностью, а следовательно, процессы рекомбинации атомов с остатком молекулы анилина или друг с другом будут протекать медленно. В связи с этим возникает предположение, что наблюдаемое здесь послесвечение анилина фиолетового цвета ( длительностью около 4 сек. [19]
Состояние возбуждения тех или иных степеней свободы, естественно, должно сказываться на кинетике реакций этих частиц. Если процессы рекомбинации атомов и радикалов, как правило, не требуют преодоления потенциального барьера, то реакции атомов и радикалов с молекулами обычно требуют энергии активации, составляющей несколько килокалорий на моль. Энергия, локализованная в той или другой форме в атомах и радикалах, очевидно, будет способствовать преодолению энергетического барьера и, следовательно, повышать скорость реакций таких частиц с молекулами. Избыточная энергия, которую могут уносить эти частицы, может достигать довольно больших ( по химическим масштабам) значений. [20]
В процессе рекомбинации атома А с двухатомным радикалом ВС при линейном расположении всех трех атомов в момент столкновения Аи ВС энергия относительного движения, в отличие от столкновения двух атомов, очевидно, не будет сосредоточена на одной связи А - В, а распределится между двумя валентными нормальными колебаниями квазимолекулы. [21]
Следовательно, при нормальной температуре бимолекулярный закон рекомбинации атомов ( при ударной стабилизации) должен наблюдаться лишь при давлениях в десятки тысяч атмосфер и более. Так как процессы рекомбинации атомов во всех случаях изучались при значительно более низких давлениях ( порядка атмосферного и ниже), то понятно, что реакция всегда следовала тримолекулярному закону. [22]
При адсорбции ионов HS ослабляется связь между поверхностными атомами, что должно облегчить проникновение водорода в металл. Гидросульфидные ионы сильно замедляют процесс рекомбинации разрядившихся атомов водорода, поэтому их концентрация на поверхности возрастает и проникновение водорода в металя усиливается. [23]
При воздействии сероводородсодержащих сред помимо коррозионных разрушений происходит наводораживание стали, приводящее в конечном счете к растрескиванию оборудования нефтяных и газовых скважин. Объясняется это тем, ч го гидросульфидные ионы сильно замедляют процесс рекомбинации разрядившихся атомов водорода, поэтому их концентрация на поверхности возрастает и проникновение водорода в металл усиливается. С увеличением концентрации сероводорода скорость проникновения водорода через металл возрастает, и при некоторой концентрации достигается насыщение. На основании этих факторов был сделан вывод, что промотирующее действие H2S носит адсорбционный характер. [24]
Например, низко расположенное состояние 3П молекулы Вг2, энергия уровней которого занимает промежуточное положение по отношению к состояниям, указанным в случаях ( Г) и ( 3), расщепляется на ряд подсостояний 0 ы, 0 -, 1м, 2и, имеющих почти одинаковую энергию. В принципе некоторые из этих состояний в соответствии с правилом корреляции могут заселяться в процессе рекомбинации атомов. [25]
По предположению Гейдона и Вольфхарда [111], возбуждение атомов металлов в пламенах осуществляется за счет энергии процессов рекомбинации атомов и свободных радикалов. Число возбужденных атомов примеси может соответствовать температуре пламени, но может и значительно превосходить равновесное значение. Это особенно характерно для низкотемпературных и разреженных пламен, в которых концентрация атомов и свободных радикалов намного превышает равновесную. [26]
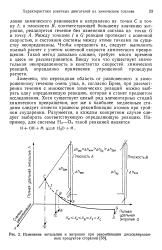 |
Изменение энтальпии и энтропии при рекомбинации диссоциированных продуктов сгорания. [27] |
Замечено, что переходная область от равновесного к замороженному течению очень узка, и, согласно Брэю, при рассмотрении течения с множеством химических реакций можно выбрать одну определяющую реакцию, которая и станет предметом исследования. Хотя существует целый ряд элементарных стадий химического превращения, все же к наиболее медленным стадиям следует отнести процессы рекомбинации атомов при тройном соударении. Разумеется, в каждом конкретном случае следует выбирать соответствующую определяющую реакцию. [28]
Для получения одноатомного водорода обычно пользуются холодным электроразрядом, пропускаемым через разреженный до 0 5 лл водород в длинной трубке со впаянными на концах металлическими электродами. Трубка должна быть длиной до 2 м, для того, чтобы каталитическое влияние металлических электродных поверхностей, способствующих соединению атомов в молекулы, не распространялось на среднюю часть трубки, где и можно в этих условиях наблюдать свободные атомы в концентрации до 20 %; чтобы стеклянные стенки трубки меньше способствовали процессу рекомбинации атомов, поверхность стенок смачивают фосфорной кислотой. [29]
Существование свободных атомов и радикалов было доказано различными методами. Так, в реакционную смесь вводят специальные зонды, снабженные чувствительными малоинерционными термопарами, покрытыми катализаторами. На поверхности таких катализаторов происходят процессы рекомбинации атомов и радикалов, сопровождающиеся значительным выделением тепла. Например, катализатор ZnOCr2O3 ускоряет реакцию рекомбинации атомов водорода. [30]
Страницы: 1 2 3