Процесс - синтез - углеводород
Cтраница 3
Хэгга ( карбид железа), применяемый в процессе синтеза углеводородов из окиси углерода и водорода. [31]
Оба катализатора - железный и кобальтовый - в процессе синтеза углеводородов способны переводить кислород окиси углерода в кислород воды и углекислоты. При одинаковых условиях синтеза ( температура и состав газа) железные катализаторы проявляют большую склонность к образованию углекислоты, а кобальтовые и никелевые катализаторы - к образованию воды. Эти результаты, типичные для железных и кобальтовых катализаторов, могут быть изменены при помощи реакции образования СО2 и Н2 из водяного газа, вызывающей изменение парциальных давлений различных реагирующих компонентов. При низких температурах синтеза достижение условий равновесия, соответствующих реакции образования СО2 и Н2 из водяного газа, происходит очень медленно. [32]
В будущем для этого, разумеется, можно использовать процесс Фишера-Трошпа синтеза Углеводородов. Масляный альдегид и к-бутанол вырабатывают не только в процессе окисления, но и ( в крупном масштабе) из этанола через ацетальдегид. По-видимому, бутилпроизводные оксосинтеза могут конкурировать с продуктами, получаемыми конденсацией ацетальдегида; во всяком случае две крупные фирмы применяют оксосинтез. [33]
В связи с большой чувствительностью катализаторов, применяемых в процессе синтеза углеводородов, к отравлению, к качеству исходного синтеза-газа предъявляются весьма жесткие требования. Синтез-газ, практически, не должен содержать пыли, смолообразующих углеводородов, каких-либо сернистых и цианистых соединений. [34]
Превращение металла в карбид во всем объеме катализатора в процессе синтеза углеводородов наблюдается только в случае железных катализаторов. Образование карбидов, возрастающее параллельно с возрастанием активности железных катализаторов, может оказывать значительное влияние на структуру катализатора и его поверхность. Тем не менее образование карбида оказывается, повидимому, недостаточным для наличия каталитической активности. [35]
Таким образом, следует предположить, что совмещение газогенераторов ТЭС с процессом синтеза углеводородов возможно. [36]
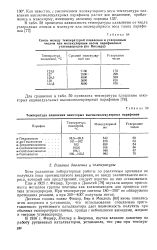 |
Температура плавления некоторых высокомолекулярных парафинов. [37] |
Еще в 1925 г. Фишер, Тропш и Дильтей [79] изучали вопрос пригодности металлов группы платины как катализаторов для процесса синтеза углеводородов. [38]
Полученный экспериментальный материал позволил установить некоторые закономерности промотирования и формирования этих катализаторов, что является базой для дальнейшей разработки процесса синтеза углеводородов и познания сущности каталитического действия железных катализаторов. [39]
Предметом многочисленных исследований оказался также так называемый оксо-процесс ( гидроформилирование олефинов и спиртов), открытый Реленом [21] в 1938 г. и являющийся важным производным от процесса синтеза углеводородов по Фишеру-Тропшу. [40]
Как упоминалось выше, имеются видоизменения процесса синтеза, направленные в сторону получения кислородных соединений. Процесс синтеза кислородных соединений из окиси углерода и водорода был разработан еще ранее процесса синтеза углеводородов и проводился при давлении порядка 150 am и температуре 400 с использованием железных катализаторов, активированных щелочами. В этом процессе получается. Суммарный выход первичных [ продуктов составляет 100 - 120 г / м3 газа. [41]
Как упоминалось выше, имеются видоизменения процесса синтеза, направленные в сторону получения кислородных соединений. Процесс синтеза кислородных соединений из окиси углерода и водорода был разработан еще ранее процесса синтеза углеводородов и проводился при давлении порядка 150 am и температуре 400 с использованием железных катализаторов, активированных щелочами. В этом процессе получается продукт, названный син-толом и состоящий из кислородсодержащих соединений и углеводородов. Суммарный выход первичных продуктов составляет 100 - 120 г / м3 газа. [42]
Как упоминалось выше, имеются видоизменения процесса синтеза, направленные в сторону получения кислородных соединений. Процесс синтеза кислородных соединений из окиси углерода и водорода был разработан еще ранее процесса синтеза углеводородов и проводился при давлении порядка 150 am и температуре 400 с использованием железных катализаторов, активированных щелочами. В этом процессе получается продукт, названный синтолом и состоящий из кислородсодержащих соединений и углеводородов. Суммарный выход первичных продуктов составляет 100 - 120 г / м3 газа. [43]
Процесс может осуществляться как в стационарном, так и в кипящем слое катализатора. Катализаторы процесса синтеза углеводородов из СО и Н2 готовятся на основе никеля, железа, кобальта, рутения, родия и других металлов VIII группы с различными добавками. [44]
Распределение компонентов в продуктах синтеза на основе HZ и СО почти во всех случаях определяется кинетикой. Большая стабильность метана приводит к значительным его выходам при различных условиях процесса на разнообразных катализаторах, что вызывает серьезные осложнения, когда необходимо получение жидких углеводородов. Трудности в достижении желаемой селективности вытекают из механизма синтеза углеводородов, а именно - из особенностей процесса полимеризации. Однако опыт проведения каталитических процессов учит, что положение максимума продукционного распределения может быть сдвинуто, а само распределение несколько сужено посредством изменения рабочих параметров или состава катализатора. Желательно для каждого специфичного процесса проводить дальнейшие исследования и разработки катализаторов синтеза. Аналогично, усовершенствование сероустойчивых катализаторов, способных к работе при концентрациях H2S 10 - 1000 млн-1, должно очень существенно повысить эффективность процесса синтеза углеводородов. [45]
Страницы: 1 2 3 4