Процесс - стеклообразование
Cтраница 3
Иной вид имеют кривые / - 5 - 6 и / - 5 - 4, характеризующие выделение тепла при процессе стеклообразования. В этом случае жидкое состояние сохраняется до более низкой температуры - температуры стеклования ( Т) и на отрезке 1 - 2 - 5 жидкость успевает выбросить значительно больше тепла, чем на отрезке / - 2 кривой кристаллизации. Таким образом, при некоторой температуре Т разность н теплосодержании кристаллического ( кривая 1 - 2 - 3 - 4) и стеклообразного ( кривая 1 - 2 - 5 - 6) тела уже значительно меньше, чем можно было бы ожидать, судя по выделившейся скрытой теплоте кристаллизации. Однако теплоемкость стеклообразного тела может быть больше теплоемкости кристаллического; поэтому возможна кривая 1 - 2 - 5 - 4, показывающая, что при некоторой температуре То теплосодержание обеих форм твердого тела станет одинаковым, что соответствует истинному термодинамическому равновесию кристаллической и стеклообразной фаз. Таким образом, при температурах значительно ниже температуры стеклования стеклообразное состояние и с энергетической точки зрения можно рассматривать как закономерное, равновесное состояние. [31]
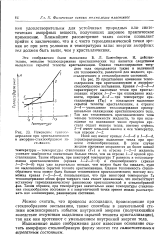 |
Изменение теплосодержания при кристаллическом и аморфно-стеклообразном застывании. [32] |
Иной вид имеют кривые / - 5 - 6 и / - 5 - 4, характеризующие выделение тепла при процессе стеклообразования. В этом случае жидкое состояние сохраняется до более низкой температуры - температуры стеклования ( Т -) и на отрезке 1 - 2 - 5 жидкость успевает выбросить значительно больше тепла, чем на отрезке 1 - 2 кривой кристаллизации. Таким образом, при некоторой температуре Т разность в теплосодержании кристаллического ( кривая 1 - 2 - 3 - 4) и стеклообразного ( кривая 1 - 2 - 5 - 6) тела уже значительно меньше, чем можно было бы ожидать, судя по выделившейся скрытой теплоте кристаллизации. Однако теплоемкость стеклообразного тела может быть больше теплоемкости кристаллического; поэтому возможна кривая / - 2 - 5 - 4, показывающая, что при некоторой температуре То теплосодержание обеих форм твердого тела станет одинаковым, что соответствует истинному термодинамическому равновесию кристаллической и стеклообразной фаз. Таким образом, при температурах значительно ниже температуры стеклования стеклообразное состояние и с энергетической точки зрения можно рассматривать как закономерное, равновесное состояние. [33]
Указанные формальные признаки стеклообразного состояния не дают представления о природе стекол, о том, какова же структура их и какую роль в процессе стеклообразования играют межмолекулярные и межчастичные силы. [34]
При скорости повышения температуры наплавления эмалей, большей, чем это принято регламентом, создаются условия интенсивного ( взрывообразного) удаления влаги, затормаживается полное прохождение процессов стеклообразования, усадки и растекания эмалевого слоя. [35]
Основными ускорителями, применяемыми при варке стекла являются фториды Na2SiF6, CaF2 и др. Присутствие фтора в количестве 0 5 - - 1 % в шихте снижает температуру завершения реакций силикатообразования на 200 С благодаря появлению жидкой фазы при низких температурах. Процесс стеклообразования ускоряется также в результате воздействия паров фтора на кристаллическую решетку кремнезема, а также благодаря повышению теплопроводности шихты. [36]
На второй стадии - стеклообразования - при повышении температуры до 1150 - 1200 С завершаются реакции силикатообразования, образуется неоднородная по составу, пронизанная большим количеством газовых пузырьков стекломасса, а не прореагировавшие зерна кварца, количество которых достигает 25 %, и другие компоненты растворяются в силикатном расплаве. Процесс стеклообразования протекает в 8 - 9 раз медленнее, чем силикатообразование. [37]
Расплавы представляют собой черную, обуглившуюся массу. Процессу стеклообразования препятствуют, по-видимому, остатки углерода, образующегося при обугливании ацетатного аниона. [38]
Для объяснения этого несоответствия, как нам кажется, можно предположить, что жесткие трехмерносимметричные ковалентные связи, характерные для халькогенидов элементов главных трех подгрупп периодической системы, могут сохраняться в расплаве. Тогда они затрудняют процесс стеклообразования в связи с их высокой прочностью и пространственной трехмерной симметрией, препятствующей образованию неупорядоченных сплетений. [39]
Только коренные структурные изменения в веществе приводят к фазовым превращениям, в то время как в ряде случаев, о которых будет речь впереди, переход из одного агрегатного состояния в другое может и не сопровождаться фазовым переходом. Это особенно относится к процессам стеклообразования и к характеристике поведения стеклообразных, или аморфных, тел. [40]
Третий путь - стеклообразование в тончайшем слое, при котором нанесение раствора осуществляют на холодные поверхности твердых тел, а затем проводят быстрое нагревание образцов до образования стекловидной пленки. Здесь процесс разложения солей и процесс стеклообразования следуют непосредственно один за другим. [41]
В начале синтеза силикатов образуются моносиликаты. Последующее растворение зерен кварца в моносиликатах рассматривается как процесс стеклообразования, идущий с малой скоростью. [42]
Однако следует иметь в виду, что перевод монометаллических расплавов в стеклообразное состояние очень труден. Сплавление элементов друг с другом, особенно металлов с металлоидами, значительно облегчает процесс стеклообразования. [43]
Согласно структурно-анионной кинетической концепции Н. М. Бобковой, силикатное стекло необходимо рассматривать как совокупность различных по составу и строению кремнекислород-ных комплексов, но с преобладанием тех структурных группировок, которые отвечают наиболее термодинамически устойчивому соединению при переходе данного состава в расплавленное и стеклообразное состояние и находятся в соответствии с положением фигуративной точки состава на диаграмме состояния системы. Силикатным стеклам присуща микрогетерогенная структура как следствие неоднородности исходного расплава, предопределяемой кинетическими особенностями процесса стеклообразования. Структурная дифференциация в расплаве вызвана несовместимостью по структурно-геометрическим условиям образующихся кремнекислород-ных комплексов и определяется кристаллохимическими параметрами входящих в состав стекла катионов. [44]
Как известно, Н. А. Торопов I1 ] впервые экспериментально наблюдал, что при нагревании содовой шихты уже при температурах порядка 700 происходит перерождение кварца в кристобалит. В более поздней работе О. К. Ботвинкина и Е. М. Шилькова [2] показано, что растворению кварца в процессе стеклообразования предшествует превращение его в кристобалит. [45]
Страницы: 1 2 3 4