Процесс - хлорирование - углеводород
Cтраница 2
Большой практический интерес представляет процесс хлорирования углеводородов хлористым водородом-так называемое гидрохлорирование. [16]
При выделении хлористого водорода из процессов хлорирования углеводородов его обычно отделяют от органической фазы путем частичной конденсации газообразного потока при давлении близком к атмосферному. Это требует сильного охлаждения, в частности использования сжиженных газов, таких как жидкий этилен, при низких температурах, например - 50 - - 85 С. [17]
Окислительное хлорирование ( или оксихлорирование) - процесс хлорирования углеводородов, протекающий при участии окисляющих агентов, в качестве которых обычно используют кислород, в частности кислород воздуха. [18]
С точки зрения цепного радикального механизма хлорирования хорошо объясняются побочные реакции, наблюдающиеся в процессе хлорирования углеводородов, например образование С2С16 и С2С14 при хлорировании метана в условиях высоких температур. [19]
Значительный интерес для дальнейшего развития хлорорганической промышленности представляет изучение реакций деструктивного хлорирования полихлорпроизводных углеводородов, образующихся в качестве побочных продуктов во всех процессах хлорирования углеводородов. Деструктивное хлорирование полихлорэтанов, полихлорпропанов и других позволяет получать с высокими выходами четыреххлористый углерод, перхлорэтилен и другие стабильные хлорпроизводные. До настоящего времени работы в области деструктивного хлорирования у нас ограничивались лишь незначительным числом чисто прикладных вопросов, изученных Энглиным и другими, и практически совершенно не затрагивались теоретические стороны этого процесса. [20]
Это положение требует усиления темпов внедрения научных достижений в промышленную практику создания хорошей опытно-промышленной базы, а также более широкого размаха и глубины научно-исследовательских работ в области изучения процессов хлорирования углеводородов и превращений хлорпроизводных. До настоящего времени для целого ряда хлорорганических продуктов отсутствуют эффективные методы их получения, основанные на использовании углеводородов нефтяных газов. [21]
Наряду с исчерпывающим хлорированием, обычно осуществляемым при более или менее высоких температурах, имеет место деструктивное хлорирование - хлоринолиз. Под хлоринолизом обычно понимают процесс хлорирования углеводорода ( или любого другого органического соединения) в условиях, вызывающих разрыв С - С-связей и приводящих к образованию хлорпроизводных с меньшим числом атомов углерода, чем в исходном веществе. [22]
 |
Схема регулирования уровня. [23] |
Регуляторами непрерывного действия являются устройства, непрерывно поддерживающие постоянство заданных физических параметров. Например, в производстве хлорбензола процесс хлорирования углеводородов протекает при определенном температурном режиме, и увеличение температуры на 10 С может привести к взрыву. Поэтому в хлораторах устанавливают электронно-пневматические регуляторы непрерывного действия, которые, регулируя количество подаваемого бензола, поддерживают заданную температуру. [24]
 |
Схема опытной абсорбционной установки получения соляной кислоты с типичными показателями для одного из опытов. [25] |
Хотя процесс абсорбции концентрированных паров НС1, применяемый в производстве соляной кислоты, выходит из рамок настоящей книги, извлечение следов НС1 из хвостовых газов такого процесса, несомненно, отно - сится к области очистки газа. Очистка газа от следов НС1 особенно важна в производстве соляной кислоты как побочного продукта процессов хлорирования углеводородов, так как выделяющийся в ходе этих процессов НС1 сопровождается большим объемом инертных компонентов. Описываемый в обзоре методов производства соляной кислоты [32] абсорбер для очистки хвостовых газов имеет обычную конструкцию и заполняется керамической насадкой. Абсорбер работает при расходе жидкости около 2 4 м3 / ч м2 и выше и скорости газа 0 3 - 0 9 м / сек. Абсорберы обычно работают под вакуумом; газ просасывается вытяжным вентилятором на линии отходящего газа. [26]
Для получения CCU и СС1а - СС12 высокотемпературное хлорирование метана проводят в двух последовательно соединенных реакторах [73] или в реакторе с несколькими зонами [74], В первый реактор вводят смесь С12 и СН4 при 650 С с высокой скоростью, во втором реакторе к охлажденным до 450 С продуктам реакции добавляют в трех местах нагретый до 630 С метан. С точки зрения цепного радикального механизма хлорирования хорошо объясняются побочные реакции, наблюдающиеся в процессе хлорирования углеводородов, например образование С2С1в и СС12СС12 при хлорировании метана в условиях высоких температур. [27]
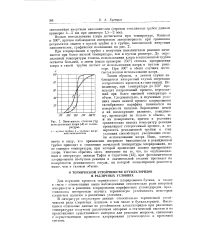 |
Зависимость степени ( % использования хлора ( А от температуры. [28] |
В литературе отсутствуют данные относительно термической устойчивости ряда хлористых алкилов, в том числе и бутилхлоридов. Имеющиеся отдельные данные по устойчивости алкилхлоридов при различных температурах получены различными авторами в статической системе и не представляют существенного интереса для решения вопросов, связанных с осуществлением процессов хлорирования углеводородов в проточной системе. [29]
Большой тепловой эффект реакций хлорирования и малое изменение энтропии обусловливают отрицательное значение свободной энергии, которое приводит к большим константам равновесия практически при всех температурах. Поэтому реакции хлорирования углеводородов всегда необратимы. Возможно, что это обстоятельство и явилось причиной крайне бедного освещения в литературе систематических данных по термодинамике процессов хлорирования углеводородов. Между тем, рассмотрение значений энтальпии и энтропии и сопоставление констант равновесия семейства реакций может привести к некоторым обобщениям. [30]
Страницы: 1 2 3