Медленный процесс
Cтраница 2
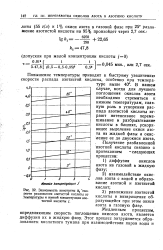 |
Зависимость константы рости разложения азотистой кислоты от. температуры и ионной концентрации азотистой кислоты /. [16] |
Медленным процессом, определяющим скорость поглощения окислов азота, является диффузия их в жидкую фазу. [17]
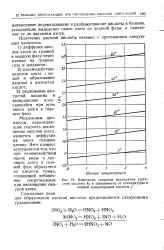 |
Константы скорости разложения азотистой кислоты &. в зависимости от температуры и ионной концентрации кислоты /. [18] |
Медленным процессом, определяющим скорость поглощения окислов азота, является диффузия их через газовую пленку. [19]
Наиболее медленным процессом, определяющим скорость реакции окисления водорода, является реакция между атомом водорода и кислородом, так как требует наибольшей энергии активации. [20]
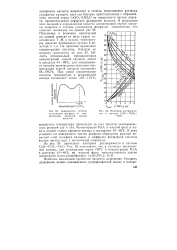 |
Зависимость степени разложения фосфата от концентрации исходной серной кислоты.| Изотермы растворимости в системе СаО - Р2О5 - - Н2О. [21] |
Наиболее медленным процессом является дозревание. [22]
Наиболее медленным процессом является дозревание. Ускорить дозревание можно охлаждением суперфосфатной массы и испарением из нее воды, что способствует кристаллизации монокальцийфосфата и повышает скорость реакции ( б) вследствие увеличения концентрации Н3РО4 в растворе. С этой целью на складе перемешивают и распыляют суперфосфат. [23]
Наиболее медленным процессом является первая стадия, скорость которой зависит - от размера капель, что определяет скорость их разогрева. [24]
Наиболее медленным процессом является первая стадия скорость которой зависит от размера капель, что определяет скорость их разогрева. [25]
 |
Схема производства суперфосфата непрерывным способом. [26] |
Наиболее медленным процессом является дозревание. Ускорить дозревание можно охлаждением суперфосфатной массы и испарением из нее воды, что способствует кристаллизации монокальций-фосфата и повышает скорость реакции ( б) вследствие увеличения концентрации Н3РО4 в растворе. Для этого на складе перемешивают и распыляют суперфосфат. [27]
Наиболее медленным процессом в данном случае является второй. [28]
Наиболее медленным процессом, определяющим скорость реакции окисления водорода, является реакция между атомом водорода и кислородом, так как требует наибольшей энергии активации. [29]
Наиболее медленным процессом, определяющим общую скорость полимеризации, является процесс активации мономера. Скорость роста цепи примерно в 10 раз больше, чем скорость активации мономера. Энергия активации мономера при полимеризации винильных соединений составляет 20 - 30 ккал / моль ( в присутствии катализатора), а рост цепи происходит с затратой энергии порядка 4 - 6 ккал / моль. [30]
Страницы: 1 2 3 4