Реальный процесс - окисление
Cтраница 1
Реальные процессы окисления представляют собой реакции с несколькими промежуточными продуктами, последовательно или параллельно превращающимися в ходе реакции. Поэтому модели цепных вырожденно-разветвленных реакций с одним промежуточным продуктом, рассмотренные выше, лишь первое приближение к реальным процессам. Следующее, более точное приближение - - модели цепных вырожденно-разветвленных реакций с несколькими промежуточными продуктами. [1]
Реальные процессы окисления представляют собой реакции с несколькими промежуточными продуктами, последовательно или параллельно превращающимися в ходе реакции. Поэтому модели цепных вырожденно-разветвленных реакций с одним промежуточным продуктом, рассмотренные выше, лишь первое приближение к реальным процессам. Следующее, более точное приближение - модели цепных вырожденно-разветвленных реакций с несколькими промежуточными продуктами. [2]
В реальных процессах окисления углеводородов образование свободных радикалов может происходить по самым разнообразным реакциям. Поэтому целесообразно рассмотреть модель цепной реакции, в которой вырожденное разветвление происходит несколькими путями. [3]
В реальных процессах окисления металлов часто наблюдаются как нарушения приведенных выше зависимостей Ag / ( т) вследствие ряда факторов, осложняющих процесс ( нарушение сплошности пленки за счет роста внутренних напряжений и др.), так и более сложные зависимости, которые описывают процесс роста окисной пленки во времени. [4]
В реальных процессах окисления металлов часто наблюдаются нарушения приведенных выше зависимостей Ат / ( т) вследствие ряда факторов, осложняющих процесс ( нарушение сплошности пленки внутренними напряжениями, возникающими при росте защитной пленки или изменении температуры, и др.), а также более сложные зависимости, которые описывают процесс роста окисной пленки во времени. [5]
Приближение модельных систем к реальным процессам окисления достигается усложнением моделей, учитывающих наличие нескольких промежуточных продуктов, изменение состава радикалов в ходе реакции и накопление продуктов, ускоряющих распад гидроперекисей. [6]
Такие модели, несмотря на весьма упрощенное отображение реальных процессов окисления, хорошо передают главные особенности этих процессов как цепных реакций с вырожденными разветвлениями. В настоящем разделе рассмотрены другие теоретически возможные модели цепных вырожденно-разветвленных реакций. [7]
Хотя нами и не рассмотрены другие возможные механизмы окисления метана ( это не являлось задачей настоящей работы), но перечисленные результаты, которые не были заложены заранее в программу расчетов, показывают, что механизм табл. 2 является по крайней мере одним из правильно отражающих совокупность и стадийную последовательность реакций реального процесса окисления метана. [8]
Это обстоятельство сказывается на кинетике процесса окисления. Реальные процессы окисления весьма сложны по своему механизму, в них принимают участие разнообразные молекулярные продукты и различные свободные радикалы. Теоретическое рассмотрение таких сложных реакций необходимо начинать с простых кинетических моделей, в которых принимаются во внимание главные особенности рассматриваемого класса реакций. Следовательно, кинетическая модель реакции представляет собой упрощенную схему механизма процесса, отражающую главные черты исследуемого класса реакций. Если выбранная модель правильно отражает механизм данной группы реакций, то должно наблюдаться соответствие между кинетикой реальных процессов и кинетическими кривыми, полученными путем расчета. Использование кинетических моделей при изучении химических реакций помогает всесторонне изучить их механизм, сопоставить выводы теории с опытом, установить общие закономерности для изучаемых реакций. [9]
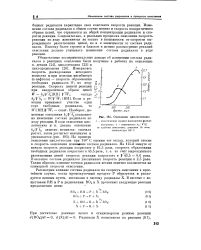 |
Окисление циклогексана. [10] |
Изменение состава радикалов в общем случае меняет и скорость квадратичного обрыва цепей, что отражается на общей концентрации радикалов и скорости реакции. Следовательно, в реальных процессах окисления скорость реакции по ходу изменяется не только в зависимости от скорости вырожденного разветвления цепей, но и в зависимости от состава радикалов. Поэтому более строгое и близкое к истине рассмотрение реакций окисления должно учитывать изменение состава радикалов в ходе реакции. [11]
Нам все еще приходится прибегать к различным механизмам, которые нужно рассматривать лишь как предельные случаи и которые при удачном сочетании дают только приближенную картину встречающихся на практике реальных процессов окисления. Подобных предельных механизмов существует множество, а главные достижения за прошедшее десятилетие сводятся к объяснению начальных стадий окисления вообще и долговременного поведения некоторых переходных металлов ( титан, ниобий), в частности. Практически наиболее важным и теоретически лучше других обоснованным механизмом окисления все еще остается данная Карлом Вагнером трактовка параболического окисления в области толстых окисных пленок. Прочие же предлагавшиеся механизмы требуют дальнейшего уточнения, а некоторые из них, вероятно, даже лишены смысла. [12]
С появлением адипиновой кислоты кобальт начинает частично выпадать в осадок в виде адипата кобальта. Как видно из изложенного, воздействие стеарата кобальта на реакцию окисления циклогексана различно на различной стадии ее развития. В первой стадии двухвалентный кобальт, окисляясь в трехвалентный, индуцирует окисление циклогексана. Во второй стадии катализатором является трехвалентный кобальт, а двухвалентный кобальт тормозит окисление. На третьей стадии кобальт в обоих состояниях является катализатором, инициируя цепи. Двойственная роль двухвалентного кобальта в реальном процессе окисления циклогексана проявляется в том, что катализатор в последовательных стадиях развития процесса выполняет функции то положительного, то отрицательного катализатора. Интересно отметить, что торможение в образовании спирта кончается раньше, чем торможение в образовании кетоиа. Было установлено, что при определенной концентрации стеарата кобальта образование спирта о второй стадии пе тормозится, а образование ке-тона заторможено. [13]
Страницы: 1