Окислительный восстановительный процесс
Cтраница 3
В физико-химическом анализе применяется измерение электродвижущей силы, возникающей в гальванических цепях. Отличительной особенностью гальванических цепей является протекание окислительных и восстановительных процессов на двух электродах, пространственно отделенных друг от друга. Вследствие раздельного протекания окислительно-восстановительных реакций электроды приобретают разные электрические потенциалы. Электродвижущая сила цепей при проведении процессов в условиях обратимости равна разности электродных потенциалов. ЭДС численно измеряется в вольтах. С термодинамическим потенциалом она связана соотношением AZ nFE, где п - заряд ионов; F - число Фарадея; Е - ЭДС. [31]
В тесной связи с вопросом о делокализации электрона в пределах одной молекулы находится и вопрос о возможности межмолекулярного переноса электрона. Наиболее хорошо изученными реакциями такого рода являются многочисленные окислительные восстановительные процессы - взаимные превращения частиц, способных изменять величину своих электрических зарядов. [32]
Таким образом, электрофилы и нуклеофилы в органических реакциях можно рассматривать соответственно как акцепторы или доноры электронных пар, принимающие их от одних атомов или отдающие их другим атомам; такими атомами чаще всего являются атомы углерода. Очевидно, что электрофильные и ну-клеофильные реакции можно рассматривать также как частный случай окислительных и восстановительных процессов, поскольку электрофилы являются акцепторами электронов, а нуклеофилы - донорами электронов. [33]
Таким образом, электрофилы и нуклеофилы в органических реакциях можно рассматривать соответственно как акцепторы или доноры электронных пар, принимающие их от одних атомов или отдающие их другим атомам; такими атомами чаще всего являются атомы углерода. Очевидно, что электрофильные и нуклеофильные реакции можно рассматривать также как частный случай окислительных и восстановительных процессов, поскольку электрофилы являются акцепторами электронов, а нуклеофилы - донорами электронов. [34]
Чтобы ясно указать место, которое фермент Шардингера занимает в группе ферментов и отмстить его полную аналогию с пероксидазой, Бах предложил дать ему название пергидридаза. Насколько можно предвидеть, пероксидаза и пергидридаза окажутся важнейшими, если не единственно важными, из тех ферментов, которые принимают непосредственное участие в окислительных и восстановительных процессах, совершающихся в живых организмах. [35]
Книга представляет собой обзор процессов неф ехимиче-ского синтеза. В ней рассматриваются основные виды сырья для нефтехимического синтеза, а также приводятся расчеты технологического оформления процессов. Особое внимание уделено термическим, окислительным, восстановительным процессам, процессам галоидирования, нитрования и сульфирования. В книге собран и систематизирован обширный литературный материал. В русском переводе опущены разделы о полимеризации и поликонденсации и простейшие технологические расчеты, так как эти вопросы достаточно полно освещены в отечественной литературе. [36]
Книга представляет собой обзор процессов нефтехимического синтеза. В ней рассматриваются основные виды сырья для нефтехимического синтеза, а также приводятся расчеты технологического оформления процессов. Особое внимание уделено термическим, окислительным, восстановительным процессам, процессам галоидирования, нитрования и сульфирования. В книге собран и систематизирован обширный литературный материал. В русском переводе опущены разделы о полимеризации и ноликонденсации и простейшие технологические расчеты, так как эти вопросы достаточно полно освещены в отечественной литературе. [37]
 |
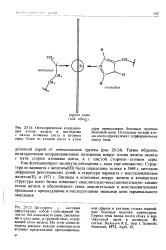
Схема окислительно-восстановительной цепи. [38] |
Электрическая энергия возникает за счет окисления ионов олова и восстановления ионов железа. В отличие от гальванических элементов ( например, медно-цинкового) здесь при окислении и восстановлении вещество металлического электрода не претерпевает никаких химических превращений. Электроды здесь являются только передатчиками электронов; окислительные и восстановительные процессы происходят только в растворе. Такие цепи носят название окислительно - восстановительных. [39]
Таким образом, октаэдрические координационные положения вокруг атома железа заняты с пяти сторон атомами азота, а с шестой стороны-атомом серы. Как функционирует молекула цитохрома с, пока еще неизвестно. Структура ее варианта с железом ( Ш) была определена только в 1969 г. методом дифракции рентгеновских лучей, а структура варианта с восстановленным железом ( П) - в 1971 г. Лиганды в комплексе вокруг железа и компактная структура всего белка изменяют окислительно-восстановительную химию атома железа и обеспечивают связь окислительных и восстановительных процессов с предыдущими и последующими звеньями цепи терминального окисления. [41]
Расчетная производительность горелок колеблется от 1 5 до 200 нм3 / час. Горелки работают при давлении природного газа от 15 до 240 мм вод. ст. и при давлении воздуха 210 мм вод. ст. Снижение давления газа от 240 до 15 мм вод. ст. уменьшает производительность горелок в 4 раза. Изменение количества, диаметра и положения отверстий в газовом наконечнике позволяет изменять длину факела - от факела максимальной длины для данной горелки до практически бесфакельного горения. Горелка применима для окислительного и восстановительного процесса сжигания топлива. [42]
В химических реакциях должно выполняться правило сохранения алгебраической суммы степеней окисления всех атомов. Именно это правило делает понятие степени окисления столь важным в современной химии. Если в ходе химической реакции степень окисления атома повышается, говорят, что он окисляется, если же степень окисления атома понижается, говорят, что он восстанавливается. В полном уравнении химической реакции окислительные и восстановительные процессы должны точно компенсировать друг друга. [43]
 |
Схема гальванического элемента Даниэля - Якоби. [44] |
Этими процессами сохраняется разность потенциалов пластинок, обеспечивающая постоянный переход электронов по проволоке от цинка к меди - электрический ток в цепи. Во внутреннем участке цепи анионы SO42 - перемещаются от медного электрода к цинковому, а катионы Zn2 и Cu2 - в обратном направлении. Суммарный процесс выражается тем же уравнением реакции Zn CuSO4 ZnSO4 Cu, что и при непосредственном взаимодействии окислительно-восстановительных систем Zn2 Zn и Cu2 Cu. Электрический ток в гальваническом элементе возникает за счет окислительно-восстановительной реакции, протекающей так, что окислительные и восстановительные процессы оказываются пространственно разделенными: на положительном электроде происходит процесс восстановления, на отрицательном - процесс окисления. [45]
Страницы: 1 2 3 4