Введение - объемистый заместитель
Cтраница 1
Введение объемистого заместителя к несущему гидроксильную группу углеродному атому существенно меняет картину. Для 2-амино - 1-фенилциклогексанола образование водородной связи возможно только в случае еа-изомера ( 64в), поскольку при введении фениль-ного радикала фиксируется конформация с экваториальной фенильной группой. У еа-изомера группы ОН и NH2 при этом сохраняют необходимое для образования внутримолекулярной водородной связи скошенное положение. В аа-изомере ( 646), в который переходит неустойчивый ее-конформер ( 64а), группы ОН и NH2 находятся в аксиальных положениях, исключающих возможность образования внутримолекулярной водородной связи. [1]
При введении объемистых заместителей конформаций цепей изменяются и переходят из ступенчатого транс-положения в гош-по-ложение. [2]
Наилучшим способом подавления нормального бимолекулярного замещения является введение объемистых заместителей к а-углеродному атому. [3]
Влияние заместителя может быть обусловлено воздействием на электронное строение ФГ или стереохимиче-скнми затруднениями, возникающими при введении объемистых заместителей в непосредственной близости к ФГ. [4]
Наличие электроноакцепторных заместителей, напр, в случае полифтор - - дикетонов, увеличивает кислотность кето-формы и способствует енолизации, а введение объемистых заместителей затрудняет ее. [5]
Кроме электронного влияния, передаваемого в основном по линии ковалентных связей, заместитель может оказывать влияние на константы ионизации органических кислот при введении объемистых заместителей, особенно на близком расстоянии от карбоксильной группы, так как эти заместители будут создавать препятствия для сольватации как кислоты, так и в большей степени соответствующего аниона. Это должно, дестабилизировать конечное состояние больше, чем исходное. [6]
Если сравнить приведенные на рис. 49 ИК-спектры цис - и транс-форм 2-аминоциклогексанола, то можно убедиться, что различие между спектрами изомеров незначительно: в спектрах обоих изомеров имеется полоса, отвечающая связанной гидроксильной группе и ( более слабая) цолоса свободной группы ОН. Введение объемистого заместителя к несущему гидроксильную группу углеродному атому существенно меняет картину. Для 1-фенил - 2-аминоциклогексанола образование водородной связи возможно только в случае 1 ыс-изомера. [7]
Соединение, соответствующее формуле I, содержит распространенную сопряженную систему тс-электронов, что предполагает копланарность обоих ядер дифенила. Если же копланарность ядер стерически затруднена вследствие введения объемистых заместителей в положения 2 и 2, то непрерывное сопряжение и, следовательно, хиноидное состояние уже не могут существовать. [8]
Это может привести к снижению устойчивости комплексов или даже к тому, что комплексы вовсе не будут образовываться. Определенное расположение донорных атомов по отношению друг к другу и введение объемистых заместителей в большем удалении от донорных атомов может препятствовать также реализации оптимальной для данного металла координации. Если, несмотря на это, образуется хелат, то говорят о вынужденной координации; в этом случае устойчивость комплекса ниже по сравнению с незамещенными реагентами. [9]
Простейшая циклическая система - циклопропан может иметь только плоскую структуру. Эта молекула не представляет каких-либо конформационных проблем, хотя при введении объемистых заместителей могут искажаться углы. [10]
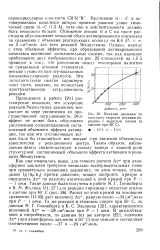 |
Влияние давления на константу скорости реакции пиридина с йодистым этилом ( в ацетоне при 40 С. [11] |
Проведенное в работе [29] рассмотрение показало, что ускорение реакций Меншуткина давлением возрастает по мере увеличения их пространственной затрудненности. Этот эффект не может быть обусловлен увеличением сольватационной составляющей объемного эффекта активации, так как эта составляющая должна была бы становиться все меньше при введении объемистых заместителей у реакционного центра. Таким образом, наблюдаемые факты свидетельствуют в пользу вывода о важной роли структурной составляющей объемного эффекта активации в реакциях Меншуткина. [12]
Если сравнить приведенные на рис. 49 ИК-спектры цис - и транс-форм 2-аминоциклогексанола, то можно убедиться, что различие между спектрами изомеров незначительно: в спектрах обоих изомеров имеется полоса, отвечающая связанной гидроксильной группе и ( более слабая) полоса свободной группы ОН. Следовательно, как в цис -, так и в гране-форме гидроксильная и аминогруппа взаимодействуют друг с другом с образованием водородной связи. Введение объемистого заместителя к несущему гидроксильную группу углеродному атому существенно меняет картину. Для 1-фенил - 2-аминоциклогексанола образование водородной связи возможно только в случае wc - изомера. [13]
В конформации кресла 1C аксиальные и экваториальные заместители меняются местами. Экваториальные гидроксильные группы легче образуют гликозидные связи, легче этерифицируются и алкилируются, чем аксиальные. Конформация глюкопиранозного цикла достаточно жесткая и не меняется после введения объемистых заместителей. [14]
Реакция Виттига кратко обсуждена в гл. Эта реакция обладает рядом преимуществ при синтезе алкенов: кислородный атом карбонильной группы замещается на этиленовую группу без всякой изомеризации; мягкие щелочные условия проведения реакции дают возможность получать такие нестойкие олефины, как каротиноиды, метилензамещенные стероиды и другие природные продукты. По существу это единственный надежный метод для превращения циклического кетона в соответственный э / сзо-циклоолефин. В этом случае синтез Гриньяра ( разд. Недостатки метода - высокая стоимость реагента и необходимость введения объемистого заместителя, который не входит в состав конечного продукта. [15]
Страницы: 1 2