Введение - ацетат
Cтраница 2
Вывод этого уравнения сделан с учетом того, что межфазовый потенциал на границе вода - смешанный растворитель постоянен для одной и той же концентрации уксусной кислоты, а диффузионный потенциал, вызываемый введением ацетатов металлов в раствор, очень незначителен в области малых концентраций солей. [16]
Окрашенное в красный цвет комплексное соединение нитрилотриуксусной кислоты с кобальтом имеет максимум поглощения при 510 ммк. При введении ацетата или тартрата поглощение усиливается, однако от избытка нитрилотриуксусной кислоты не зависит. Закон Бера соблюдается в области 0 25 - 3 75 мг / мл Со. Метод пригоден для определения высоких содержаний кобальта в сплавах. [17]
Как она изменяется при введении ацетата натрия. [18]
Из данных табл. 1 видно, что уже через 30 мин. При исследовании через 1, 2 и 4 часа после введения ацетата оказалось, что удельная активность всех исследуемых компонентов достигает максимума через 1 час. В дальнейшем удельная активность цереброзидов, ганглиозидов и липидов сохраняется на одном и том же уровне в течение 3 час. [19]
Полученное вычислением уменьшение концентрации ионов водорода вызывает недоумение. Если, предположим, в растворе соляной кислоты скорость образования водорода составляет 1 мл / с ( попытайтесь ее оценить в проводившемся Вами опыте), то после введения ацетата натрия она должна уменьшиться в 333 раза ( предполагая первый порядок реакции по водороду), и тогда 1 мл водорода образовался бы только в течение 333 с или 5 мин. Однако Вы, наверное, наблюдали, что в действительности скорость образования водорода значительно больше. [20]
 |
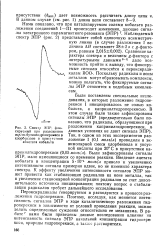
Спектр ЭПР, фиксируемый при разложении / п йт-бутилгидроперзкиси в хлорбензоле в присутствии абиетата кобальта. [21] |
Были поставлены специальные исследования, в которых разложение гидроперекиси I инициировалось не солью кобальта, а капринилгидроперекисью. Были зафиксированы сигналы ЭПР, мало изменяющиеся со временем реакции. Введение ацетата кобальта в концентрации 5 - 10 - моль / л привело к увеличению интенсивности сигнала примерно вдвое, но не изменило характера спектра. К эффекту увеличения интенсивности сигналов ЭПР может привести как стабилизация радикалов на ионе металла, так и увеличение стационарной концентрации радикалов за счет дополнительного источника инициирования; поэтому вопрос о стабилизации радикалов требует дальнейшего исследования. [22]
Добавки солей изменяют стереоселективность присоединения хлора и к фенил ацетилену в уксусной кислоте. В отсутствии солей образуется сложная смесь Е - и Z-изомерных днхлоридов в соотношении 55: 45, а также Е - и Z-изомеров продуктов сопряженного присоединения. Добавки хлорида лития резко увеличивают долю Е - днхлорида, в то время как введение ацетата лития способствует образованию Е - изомера хлоренолацетата. Все эти данные определенно указывают на образование катиноидного интермедиата в стадии, определяющей скорость присоединения галогена. Таким ингермеднатом может быть либо открытый винил-катион, либо мостиковый галоиреиневый ион. Для присоединения хлора, брома и смешанных галогенидов в уксусной кислоте был предложен достаточно сложный механизм, который в обобщенном виде представлен на нижеприведенной схеме. Согласно этой схеме, предполагается, что моноалкилацетилены и фенилацетилены присоединяют галоген по Ас. [23]
 |
Спектр ЭПР, фиксируемый при разложении тпрйти-бутилгидроперекнси 8 хлорбензоле в присутствии абиетата кобальта. [24] |
Были поставлены специальные исследования, в которых разложение гидроперекиси I инициировалось не солью кобальта, а капринилгидроперекисью. Были зафиксированы сигналы ЭПР, мало изменяющиеся со временем реакции. Введение ацетата кобальта в концентрации 5 - 10 - 4 моль / л привело к увеличению интенсивности сигнала примерно вдвое, но не изменило характера спектра. К эффекту увеличения интенсивности сигналов ЭПР может привести как стабилизация радикалов на ионе металла, так и увеличение стационарной концентрации радикалов за счет дополнительного источника инициирования; поэтому вопрос о стабилизации радикалов требует дальнейшего исследования. [25]
Содержание алюминия на порядок выше содержания других микроэлементов в природных водах ( 10 - 2 мг / л), поэтому он существенно влияет на показания фторидного электрода. Поэтому в присутствии алюминия зависимость электродного потенциала от рН сильно смещается. Последнее обусловлено тем, что в кислой области почти весь фторид-ион закомплексован и, лишь начиная с рН 7, фторидные комплексы алюминия гидролизуются, высвобождая фторид-ион. При более высоких рН чувствительность электрода снижается, что обусловлено сорбцией А1 ( ОН) 3 на мембране. Влияние ионов алюминия устраняют введением маскирующего буферного раствора с определенной ионной силой, равной 1 75 - 2 М, что достигается в основном введением ацетата и цитрата натрия с добавлением О. [26]
Страницы: 1 2