Другой окислительно-восстановительный процесс
Cтраница 1
Другой окислительно-восстановительный процесс, теоретически ( и практически) ограничивающий возможность существования некоторых редоксформ в водном растворе, - это процесс редоксдиспропорционирования. Редоксдиспропорционирование связано с существованием ряда ( более двух) степеней окисления рассматриваемого элемента и обусловлено специфическим способом проявления редоксамфотерности элементом в состоянии средней степени окисления. [1]
При электролизе могут происходить и другие окислительно-восстановительные процессы. [2]
В рассмотренных работах были изучены и другие окислительно-восстановительные процессы. Результаты этих исследований заставляют рассматривать механизмы многих из этих реакций с новой точки зрения. [3]
Подобные же схемы можно составить и для других окислительно-восстановительных процессов. Составление их весьма облегчает вывод уравнений реакций окисления-восстановления, в которых нередко приходится иметь дело с довольно большими коэффициентами; нахождение их обычно затрудняет начинающих. [4]
При электролизе, в зависимости от условий, могут идти и другие окислительно-восстановительные процессы. [5]
Подобные же отклонения от закона действия масс наблюдаются и при многих других окислительно-восстановительных процессах. [6]
Подобные же отклонения от закона действия масс наблюдаются и при многих других окислительно-восстановительных процессах. [7]
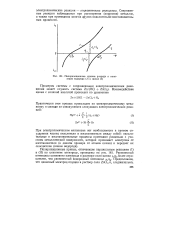 |
Поляризационные кривые разряда и ионизации водорода ( / и цинка ( 2. [8] |
Сопряженные реакции наблюдаются при растворении ( коррозии) металлов, а также при протекании многих других окислительно-восстановительных процессов. [9]
Способ рассмотрения работы элемента при помощи поляризационных кривых, конечно, не изменится, если вместо окисления-восстановления металлов на электродах будут совершаться какие-либо другие окислительно-восстановительные процессы. [10]
Так, измерение собственного потенциала металла возможно лишь в том случае, если на электроде устанавливается равновесие Me i i Me z и не происходит никаких других окислительно-восстановительных процессов. Если раствор освобожден от воздуха и потенциал электрода лежит в области А, то это условие может быть выполнено. [11]
Аналогичное образование более окисленных промежуточных соединений, обладающих повышенной окислительной активностью, по теории, предложенной известным русским химиком А. Н. Бахом, наблюдается и при многих других окислительно-восстановительных процессах. [12]
Аналогичное образование более окисленных промежуточных соединений, обладающих повышенной окислительной активностью, по теории, предложенной известным русским химиком А. Н. Бахом, наблюдается и при многих других окислительно-восстановительных процессах. Образование этих соединений, условно называемых первичными окислами, является причиной сопряженных реакций окисления - восстановления. [13]
Аналогичное образование более окисленных промежуточных соединений; обладающих повышенной окислительной активностью, по теории, предложенной известным русским химиком А. Н. Бахом, наблюдается и при многих других окислительно-восстановительных процессах. Образование этих соединений, условно называемых первичными окислами, является причиной сопряженных реакций окисления - восстановления. [14]
Часто на поверхности электрода возможно одновременное протекание двух или более различных независимых электродных процессов, которые называют сопряженными реакциями. Сопряженные реакции наблюдаются при растворении ( коррозии) металлов, а также при протекании многих других окислительно-восстановительных процессов. [15]
Страницы: 1 2