Осмотический процесс
Cтраница 1
Осмотические процессы на контакте промывочной жидкости с глинистой породой детально изучены. [1]
Осмотические процессы также присущи животным тканям и клеткам. Поскольку животные клетки обычно представляют собой уплотненный слой цитоплазмы, постольку внешне осмос проявляется несколько иначе, однако принципиально картина не отличается от описанной в случае растительных клеток. Если поместить эритроциты в концентрированный раствор того или иного вещества, они вследствие экзосмоса уменьшаются в объеме, сморщиваются, что хорошо можно наблюдать под микроскопом. Когда эритроциты помещены в раствор с меньшим осмотическим давлением, чем давление клеточного раствора, наблюдается значительное увеличение объема клеток. Если эритроциты поместить в дистиллированную воду, то идет настолько интенсивный эндосмос, что в результате тургора эритроциты лопаются. Во внешнюю среду выделяется гемоглобин, благодаря чему раствор окрашивается в красный цвет. Такое явление называется гемолизом. Поэтому кровоточащие раны нельзя обрабатывать водой, так как это усиливает кровотечение. Клетки сохраняют нормальное состояние и в том случае, когда осмотическое давление внутриклеточного и внешнего раствора одинаково. [2]
Осмотические процессы и осморегуляция в животных организмах отличаются ббльшим разнообразием, чем в растительных. Внутренние растворы морских беспозвоночных изотоничны с морской водой, являющейся внешней средой. У различных животных организмов в процессе эволюции вырабатываются приспособления, позволяющие животным развиваться независимо от колебаний состава внешней среды. Так, хотя у акуловых рыб концентрация солей в крови ниже, чем концентрация их в морской воде, однако кровь акуловых изотонична с внешней средой, так как недостаток солей в крови здесь компенсируется значительной концентрацией мочевины, образующейся в результате распада белковых веществ. [3]
Осмотические процессы активно участвуют в формировании цементного камня и играют заметную роль при его работе. Практический интерес представляют такие разновидности осмоса, как термоосмос, капиллярный и обратный осмос. Доминирующим является концентрационный осмос. [4]
Если осмотические процессы рассматриваются вне связи с их влиянием на напряженное состояние испытуемых пород, т.е. без учета их возможной осмотической консолидации ( разд. [5]
Результат осмотических процессов неодинаков для обитателей разных типов водоемов. [6]
Влияние осмотических процессов на устойчивость пород в приствольной зоне скважины весьма существенно и в значительной мере предопределяет форму ствола скважины, отдаляя ее от идеализированной. Однако использование осмотических процессов может помочь в формировании ствола скважины заданной конфигурации. [7]
При осмотическом процессе растворимые в воде вещества могут создавать в покрытии и на поверхности металла осмотическое давление. Киттельберг и Элма показали, что при погружении изолированных металлических образцов в дистиллированную воду и в раствор соли ( с осмотическим давлением 30 кГ / см2) изоляционное покрытие более сильно вспучивалось в дистиллированной воде. [8]
 |
Изотермы ограниченного ( / и неограниченного ( 2 набухания.| Кинетические кривые ограниченного ( / и неограниченного ( 2 набухания. [9] |
Набухание - осмотический процесс, при котором происходит диффузия молекул растворителя в высокомолекулярное вещество. Такой односторонний процесс объясняется тем, что макромолекулы ВМС очень большие и разветвленные, благодаря чему они переплетены между собой и слабо подвержены действию теплового движения. В противоположность молекулам ВМС небольшие молекулы растворителя очень подвижны, они проникают внутрь ВМС, увеличивая его объем. [10]
Набухание - осмотический процесс, при котором происходит диффузия молекул растворителя в высокомолекулярное вещество. Такой односторонний процесс объясняется тем, что макромолекулы ВМС очень большие и разветвленные, благодаря чему они переплетены между собой и слабо подвержены действию теплового движения. В противоположность молекулам ВМС небольшие молекулы растворителя очень подвижны, они легко проникают в высокомолекулярное соединение, увеличивая его объем. [11]
Для обсуждения осмотических процессов, в которых концентрация растворенного вещества меняется, такое толкование оказывается неудобным. [12]
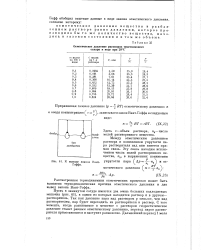 |
К выводу закона Вант - упругости пара ( Др - - п2 и ос - Гоффа. ч, 1 д. [13] |
Рассмотрением термодинамики осмотических процессов может быть выяснена термодинамическая причина осмотического давления и дан вывод закона Вант-Гоффа. [14]
В результате осмотических процессов концентрации растворов, соприкасающихся между собой через мембрану, изменяются: с, падает, а с2 возрастает. Когда обе концентрации выровняются, осмотическое проникновение растворителя из стакана А в сосуд Б прекратится - система перейдет в состояние, подвижного равновесия. [15]
Страницы: 1 2 3 4