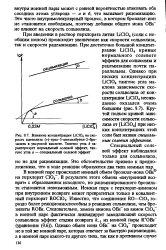
Внутримолекулярный процесс
Cтраница 1
Другие внутримолекулярные процессы рассмотрены в следующем разделе. [1]
Внутримолекулярные процессы обмена электронной, а также колебательной энергией между различными состояниями играют важную роль в фотохимическом поведении молекулы ( гл. Возможен также межмолекулярный процесс обмена энергией между двумя партнерами: при этом акцептор А, получая энергию от донора D, затем участвует в реакциях уже как электронно-возбужденная частица. Такие фотосенсибилизиро-занные процессы, в которых происходят химические превращения частиц, не поглощавших излучение, имеют большое значение в фотобиологии; они также важны для исследования фотофизических процессов. [2]
Внутримолекулярные процессы миграции атомов и атомных групп играют очень большую роль при распаде многих производных изоксазола. [3]
Такой внутримолекулярный процесс не возможен в случае а-гликозида. [4]
Это чисто внутримолекулярный процесс, в котором брозилат-ион не становится свободным, поэтому добавки общего иона OBs - не влияют на скорость сольволиза. [6]
Перегруппировка представляет собой внутримолекулярный процесс, протекающий через циклические переходные состояния; при перегруппировке смесей различных эфиров перекрестные продукты не обнаружены. Аллильные группы подвергаются инверсии при каждой индивидуальной [3,3] - миграции. [7]
Перегруппировка представляет собой внутримолекулярный процесс, протекающий через циклические переходные состояния; при перегруппировке смесей различных эфиров перекрестные продукты не обнаружены. [8]
Был предложен также внутримолекулярный процесс ( XXXVI), важный при фотолизе простых амидов в растворах, но его значение для высших амидов не выяснено. Для фотолиза в гексановых и диоксановых растворах рассматривался процесс ( XXXVII), но доказательства его протекания не очень убедительны. Он не имеет аналогов в других классах соединений и не может считаться установленным. [9]
Обрыв цепей представляет собой внутримолекулярный процесс по отношению к растущим ионным парам и является медленным, так как его энергия активации выше, чем энергия активации процесса роста цепи. Отношение скоростей процессов роста и обрыва цепи, которое представляет собой степень полимеризации, будет, следовательно, уменьшаться с ростом температуры. [10]
Следовательно, если внутримолекулярные процессы вносят определяющий вклад в процесс плавления, энтропия плавления обратно пропорциональна температуре плавления. [11]
Энтропия активации для внутримолекулярного процесса связана с вероятностью подхода двух реакционных центров одной молекулы друг к другу. Эта вероятность уменьшается ( AS приобретает большое отрицательное значение) при увеличении длины цепи. Энтальпия активации отражает напряженность переходного состояния, приводящего к образованию цикла. Значение энтальпии активации наименьшее при образовании пяти - и шестичленных циклов и несколько увеличивается при образовании более напряженных трех - и четырехчленных циклических систем. Значение Д / / 1 велико при образовании циклов среднего размера ( от восьми - до одиннад-цатичленных), что связано с пространственными взаимодействиями в кольце. Значение свободной энергии активации при образовании циклов среднего размера также велико, поэтому замыкание таких циклов затруднено. [12]
Движущая сила этого внутримолекулярного процесса замещения у атома кислорода, безусловно, заключается в образовании радикала, который одновременно является бензильным и а-алко-ксильным. [13]
Перегруппировка Стивенса является внутримолекулярным процессом, а мигрирующая группа, как было показано ранее, перемещается с сохранением конфигурации. [14]
В многоатомных молекулах происходят внутримолекулярные процессы перераспределения энергии между разл. [15]
Страницы: 1 2 3 4