Прочность - водородное соединение
Cтраница 2
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидраты остальных элементов амфотерны, причем кислотные свойства сильнее выражены у гидратов германия, а основные - у гидратов свинца. От углерода к свинцу уменьшается прочность водородных соединений RH4: CH4 - прочное вещество, а РЬН4 в свободном виде не выделено. [16]
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидраты остальных элементов амфотерны, причем кислотные свойства сильнее выражены у гидратов германия, а основные - у гидратов свинца. От углерода к свинцу уменьшается прочность водородных соединений RH4: СН4 - прочное вещество, а РЬН4 - в свободном виде не выделено. [17]
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидроксиды остальных элементов амфотерны, причем кислотные свойства сильнее выражены у германия, а основные - у свинца. От углерода к свинцу уменьшается прочность водородных соединений ЭН4: CHi - прочное вещество, а РЬН4 в свободном виде не выделен. [18]
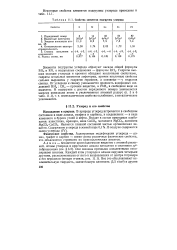 |
Свойства элементов подгруппы углерода. [19] |
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидраты остальных элементов амфотерны, причем кислотные свойства сильнее выражены у гидратов германия, а основные - у гидратов свинца. От углерода к свинцу уменьшается прочность водородных соединений RH4: СН4 - прочное вещество, а РЬН4 в свободном виде не выделено. [20]
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидроксиды остальных элементов амфотерны, причем кислотные свойства сильнее выражены у германия, а основные - у свинца. От углерода к свинцу уменьшается прочность водородных соединений RH4: СН4 - прочное вещество, а РЬН4 - в свободном виде не выделено. [21]
Гидраты высших оксидов углерода и кремния обладают кислотными свойствами, гидраты остальных элементов амфотерлы, причем кислотные; свойства сильнее выражены у гидратов германия, а основные - у гидратов свинца. От углерода к свинцу уменьшается прочность водородных соединений RH. СН - прочное вещество, а РЬН в свободном виде не выделено. [22]
Пункты 3 и 6 табл. 3.1 характеризуют металлические свойства элементов. Как видно, в подгруппе с ростом порядкового номера неметаллические свойства убывают, а металлические усиливаются. Этим объясняется уменьшение прочности водородных соединений RH3 от NH3 к BiH3, а также уменьшение прочности кислородных соединений в обратном порядке. [23]
Водородные соединения элементов подгруппы азота общей формулы ЭН3 представляют собой бесцветные газообразные вещества с характерным резким запахом. В пределах одной подгруппы с увеличением радиусов атомов при одинаковой величине зарядов притяжение элемента Э с водородом уменьшается, в связи с чем и прочность водородных соединений уменьшается от азота к висмуту. Так, если аммиак NH3 разлагается при 700 С, фосфин РН3 - при 400 С, арсин AsH3 - при 230 С, стибин SbH3 - при осторожном нагревании, то висмутин BiH3 разлагается уже при комнатной температуре. [24]
 |
Сравнительная характеристика галогенов. [25] |
По мере увеличения атомного веса физические и химические свойства галогенов закономерно изменяются. Так с водородом и металлами более активно реагирует фтор, менее активно - иод. То же наблюдается при взаимодействии галогенов со сложными веществами. Фтор чрезвычайно энергично реагирует с нагретой водой; менее активно взаимодействует с нею хлор, еще слабее иод. Как видно из таблицы, ослабление неметаллических свойств галогенов происходит по направлению от фтора к иоду. В этом направлении уменьшается прочность водородных соединений. [26]
Однако наряду со сходством галогены проявляют и различия в свойствах. Это обусловлено разными их атомными массами и неодинаковым числом электронных слоев в оболочках атомов. По мере увеличения атомной массы и числа электронных слоев физические и химические свойства галогенов закономерно изменяются. Увеличение числа электронных слоев в оболочке атома всегда приводит к ослаблению притяжения валентных электронов к ядру. Поэтому самый активный неметалл среди галогенов - фтор: его валентные электроны наиболее прочно удерживаются ядром. Как видно из табл. 3, ослабление неметаллических свойств галогенов происходит по направлению от фтора к иоду. В этом направлении уменьшается прочность водородных соединений. [27]
Страницы: 1 2