Прочность - образующееся соединение
Cтраница 1
Прочность образующегося соединения позволяет применять для маскировки мешающих ионов различные коиплексообразовзтели. Определение ванадия возможно в очень широком интервале концентраций. [1]
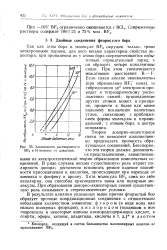 |
Зависимость растворимости BF3 в Н - пентане от давления. [2] |
Теория донорно-акцепторной связи не позволяет количественно предсказать прочность образующихся соединений. Бесспорно, что эта теория должна дополняться представлениями, заимствованными из электростатической теории образования комплексных соединений. В ряде случаев весьма существенную роль играет полярность донора; достаточно вспомнить резкое падение способности присоединения к кислотам, происходящее при переходе от аммиака к фосфину и арсину. Хотя молекула BF3 сама по себе неполярна, она способна присоединять ионы или полярные молекулы. При образовании донорно-акцепторных связей существенную роль оказывают и стереохимические условия. [3]
При невысоких температурах для реакций между твердыми или жидкими веществами тепловой эффект может служить мерой прочности образующихся соединений. [4]
Исследование равновесий в растворах комплексных соединений с применением разнообразных физико-химических методов измерения дает возможность установить химическое поведение вещества в растворе, определить состав и прочность образующихся соединений, что особенно важно для тех случаев, когда таковые не могут быть выделены из раствора. [5]
Исследование равновесий в растворах комплексных соединений с применением разнообразных физико-химических методов измерения дает возможность установить химическое поведение вещества в растворе, определить состав и прочность образующихся соединений, что особенно важно для тех случаев, когда последние не могут быть выделены из раствора. [6]
 |
Схема системы, состоящей из трех компонентов. растворителя S, соединения, содержащего комплексообразова-тель М, и соединения. [7] |
Удобно рассматривать различные варианты спектрофотометри-ческого метода на примере систем различной сложности, подразумевая, что сложность системы определяется, с одной стороны, числом и прочностью образующихся соединений, с другой, - сочетанием их оптических свойств. [8]
Кислотность среды влияет не только на скорость распада дитиокарбамината, но очень часто, ввиду малых значений констант диссоциации дитиокарбаминовых кислот, является определяющей и при образовании малорастворимых дитиокарбаминатов тяжелых металлов. Экстракция дитиокарбаминатов металлов при более низких значениях рН зависит от прочности образующегося соединения, а также от скорости образования малорастворимого дитиокарбамината металла и скорости разложения образовавшейся дитиокарбаминовой кислоты. Если скорость образования малорастворимого соединения значительно превышает скорость разложения кислоты, то наблюдается полное связывание металла в кислых средах. При соизмеримых скоростях требуется относительно большой избыток реагента. Значительно медленнее разлагаются реагенты в органическом растворителе. [9]
Глутаминовая кислота в обоих случаях способствует более полному переведению ванадия в растворимое состояние. Эта же закономерность наблюдается и при выщелачивании ванадия из почв ( табл. 3), что хорошо соответствует данным о прочности образующихся соединений. [10]
Увеличение числа циклов при прочих равных условиях приводит к упрочению комплексов. Кэльвин и Бейльс [52] доказали это, в частности, на примере салицилальдииминов. В качестве критерия прочности образующихся соединений они использовали потенциал полуволны, определенный с капельным ртутным электродом; чем отрицательней потенциал, тем прочнее комплекс. [11]
Большинство из них неустойчиво и существует только в растворах. Однако некоторая часть гидратов является настолько прочными соединениями, что при выделении растворенного вещества из раствора вода входит в состав растущего кристалла в химически связанном виде. Такие кристаллы были названы кристаллогидратами, а входящая в их состав вода - кристаллизационной. Примерами кристаллогидратов являются CuSO4 5Н20; Na2SO4 10Н2О и др. Прочность образующихся соединений определяется силами, действующими между растворителем и растворенным веществом. В настоящее время известна природа этих сил. Сольваты ( гидраты) образуются за счет ион-дипольного, диполь-ди-польного, донорно-акцепторного взаимодействия, за счет водородных связей, а также дисперсионного взаимодействия. [12]
Термодинамика не объясняет, почему при одних реакциях выделяется очень большое количество тепла, а при других меньшее. Почему кремний является лучшим раскислителем стали, чем марганец. Почему азот труднее вступает в реакции с металлами, чем кислород, а аргон вовсе с ними не реагирует. Вообще, какие свойства элементов определяют их способность вступать в химические реакции и прочность образующихся соединений. Эти и подобные им многочисленные вопросы возникают при рассмотрении любого металлургического процесса. Они затрагивают тайну самого химического превращения и связаны с природой химических тел и химической связи. Понимание этого круга вопросов невозможно без знания строения вещества. Учение о химической связи стало развиваться лишь после того, как было раскрыто строение атома. [13]
Страницы: 1