Наибольшая прочность - связь
Cтраница 2
 |
Схема полотняного переплетения.| Схема саржевого-переплетения. [16] |
Все четные нити перекрывают очередную уточную нить сверху, проходят под следующую уточную нить и снова перекрывают третью уточную нить сверху. Все нечетные нити основы проходят под первой уточной нитью, перекрывают вторую и проходят под третью уточную нить. Полотняное переплетение обеспечивает наибольшую прочность связи между нитями основы и утка. Поэтому большая часть технических тканей имеет полотняное переплетение. [17]
Все четные нити перекрывают очередную уточную пит. Все нечетные нити основы проходят под первой уточнен нитью, перекрывают вторую и проходят под третью уточную нить. Полотнянсе переплетение обеспечивает наибольшую прочность связи между нитями основы и утка. Поэтому большая часть технических тканей имеет полотняное переплетение. [18]
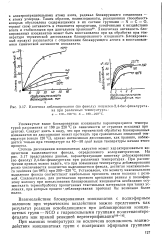 |
Кинетика деблокирования ( по фенолу голуилен-2 4-бис-фенилурета - на при различных температурил. а - 120 - 150 С. б - 180 - 220 С. [19] |
Степень диссоциации изоцианатных аддуктов может характеризоваться количеством выделившегося фенола, определяемого колориметрически. На рис. 3.17 представлены данные, характеризующие кинетику деблокирования ( по фенолу) 2 4-бис-фенилуретана при различных температурах. При рассмотрении кривых можно видеть, что при повышении температуры деблокирования резко увеличивается количество выделившегося фенола, достигая максимального значения ( до 98 %) при 200 - 220 С. Установлено, что моменту максимального выделения фенола соответствует наибольшая прочность связи волокна с резиной. [20]
На рис. 99 представлено изменение валентных состояний металлов больших периодов в зависимости от их атомного номера. Указаны валентности каждого металла в различных химических соединениях, причем валентности, соответствующие наиболее прочным соединениям, даны зачерненными значками. От I до VI групп высшей валентностью, отвечающей наиболее прочной химической связи, оказывается валентность, соответствующая номеру группы. Только у хрома наряду с шестивалентными соединениями сравнительно прочными оказываются и трехвалентные. В VII группе наибольшая прочность соединений соответствует двухвалентному марганцу, который бывает и одновалентным, однако технеций и рений дают более стабильные четырех -, шести - и семивалентные соединения. В VIII группе у железа, кобальта и никеля наибольшая прочность связи соответствует двух - и трехвалентным соединениям, а у рутения и осмия - четырехвалентным. У родия и иридия наиболее прочны трехвалентные соединения, у никеля, палладия и платины - двухвалентные, а у металлов I группы - меди, серебра и золота - устойчивы одновалентные соединения. Итак, обычные химические валентности у элементов 4-го, 5-го и 6-го периодов нарастают от 1 для калия, рубидия и цезия до 6 для хрома, молибдена и вольфрама, а затем падают до 1 у меди, серебра и золота. [21]
При нагреве устойчивость окислов снижается. По достижении определенной температуры окислы способны разлагаться на металл и кислород. На этом основано удаление окислов при пайке в вакууме и в нейтральных газовых атмосферах. Устойчивость окисла или температура его разложения определяется прочностью связи элементов в окислах. Прочность связи или способность к разложению окисла может быть приближенно оценена по теплоте образования окисла. Так, окислы благородных металлов имеют невысокие значения теплоты образования и наиболее легко разлагаются при нагреве. Окислы же легких металлов имеют наибольшую прочность связи элементов в окислах и наиболее трудно поддаются диссоциации при нагреве. [22]
Страницы: 1 2