Пути - кристаллизация
Cтраница 2
Стрелками указаны пути кристаллизации в процессе изобарического выпаривания. Из рисунков видно, что при давлениях ниже Ртах в некотором температурном интервале происходит полное выпаривание, причем при ti наступает кристаллизация одной соли, а при 4 раствор полностью выпаривается. [16]
Так как пути кристаллизации на поверхностях однократно насыщенных растворов лежат в плоскостях, проходящих через одно из трех ребер тетраэдра DA, DB или DC, то эти пути проектируются здесь в виде прямых. [17]
Построение такого пути кристаллизации, кроме того, фиксирует состав маточного раствора после окончания выделения одной соли. [18]
Касательная к пути кристаллизации тоже проходит вне треугольника SiS2S3 ( рис. XX II 1.14, в), но таким образом, что точка ее пересечения с плоскостью этого треугольника лежит против одной из вершин ( в нашем случае против вершины Ss и между продолжением сторон Зг83, S2S3); это - дважды инконгруэнтный процесс. [19]
 |
Диаграмма состояния анортита СаО - АЬОзХ X2SiO2. [20] |
Рассмотрим некоторые пути кристаллизации расплавов в системе. [21]
 |
Процесс обменного разложения солей в квадратной диаграмме. [22] |
Вследствие этого действительные пути кристаллизации могут отличаться от теоретических, соответствующих равновесному состоянию в любой момент времени. Например, в рассмотренной выше водной системе Na, Mg2 Cl -, SOf кристаллизация галита может идти не только в поле насыщения NaCl, но продолжаться некоторое время и при перемещении фигуративной точки солевого состава раствора в поле двойных солей, без их выделения в твердую фазу. [23]
Однако построение всего пути кристаллизации для точки т возможно лишь в том случае, если на диаграмме нанесены линии изменения состава жидкой фазы при кристаллизации. [25]
Выше были рассмотрены пути кристаллизации солей из морской воды и ее концентратов при изотермическом испарении. [26]
 |
Сечения /, / / и / / / тетраэдра концентраций ( 42. [27] |
Необходимо подчеркнуть, что пути кристаллизации в сечениях не могут строиться по правилам, действительным для трехкомпо-нентной системы. В четырехкомпонентной системе процесс кристаллизации прослеживается таким образом. Путь кристаллизации первичной кристаллической фазы идет по прямой от точки состава ее внутрь области кристаллизации этой фазы. Дойдя до пограничной поверхности, он продолжается по сложной кривой, лежащей на поверхности раздела областей кристаллизации двух фаз. Кривая образуется при пересечении пограничной поверхности плоскостью, проходящей через точку исходного расплава и точки составов сосуществующих на данной пограничной поверхности твердых фаз. Три твердые фазы будут выделяться по пограничной кривой, к которой примыкают области кристаллизации этих фаз. [28]
 |
Часть изотермической диаграммы растворимости взаимной системы 2NaCl - f MgSO4 rr MgCl2 Na2SO4 при О и 25. [29] |
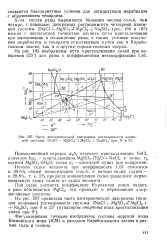
На рис. 185 изображены пути кристаллизации солей при испарении ( 25) для рапы с коэффициентом метамор. [30]
Страницы: 1 2 3 4
