Дигидроксиацетонфосфат
Cтраница 1
Дигидроксиацетонфосфат обратимо превращается в изомерный глицеральдегид-3 - фосфат. Окисление этого вещества до глицериновой кислоты-3 - фосфата является реакцией, в результате которой создается значительный запас энергии и образуется АТР из аденозиндифосфата ( ADP) и неорганического фосфата. Реакция осуществляется через смешанный ангидрид карбоновой и фосфорной кислот. Окисление на этой стадии проходит за счет превращения клеточного реагента ( кофермента) NAD в его восстановленную форму NADH ( разд. Затем глицериновая кислота-3 - фосфат изомеризуется в глицериновую кисло-ту-2 - фосфат, при элиминировании воды из которой образуется фосфат енольной формы пировиноградной кислоты. Это соединение, будучи сильным фосфорилирующим агентом, подобно предыдущей реакции образования смешанного ангидрида, переводит ADP в АТР, само превращаясь при этом в пировиноград-ную кислоту. [1]
Дигидроксиацетонфосфат является, как известно, одним из промежуточных продуктов гликолиза, превращающимся в глицеральдегид-3 - фосфат. [2]
Дигидроксиацетонфосфат NADH Пальмитиновая кислота Олеиновая кислота ЗАТР СТР Холин 4Н2О - - Фосфатидилхолин Ч - NAD 2AMP ADP - I - CMP 5Pf H; 7 молекул ATP на 1 молекулу фосфатидилхолина. [3]
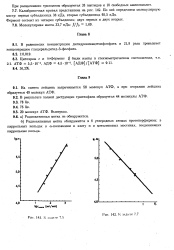 |
К задаче.| К задаче. [4] |
В равновесии концентрация дигидроксиацетонфосфата в 21 8 раза превышает концентрацию глицеральдегид-3 - фосфата. [5]
В равновесии значительно преобладает дигидроксиацетонфосфат, однако на следующей стадии гликоли-тического пути в реакцию вовлекается именно D-глицеральдегид-фосфат, который в присутствии триозофосфат-дегидрогеназы превращается [258] в 1 3-дифосфат глицериновой кислоты. [6]
Равновесие данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95 % дигидроксиацетонфосфата и около 5 % глице-ральдегид-3 - фосфата. В последующие реакции гликолиза может непосредственно включаться только один из двух образующихся триозофосфатов, а именно глицеральдегид-3 - фосфат. Вследствие этого по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы ди-гидроксиацетонфосфат превращается в глицеральдегид-3 - фосфат. [7]
ТРИОЗОФОСФАТИЗОМЕРАЗА ( О-глицеральдегид - 3-фос-фат кетол-изомераза), фермент класса изомераз, катализирующий обратимую р-цию изомеризации О-глицеральде-гид - 3-фосфата в дигидроксиацетонфосфат в процессе гликолиза. [8]
GAPDH); Е3 - а-глицерофосфат-дегидрогеназа ( aGPDN); Е4 - фосфатглицераткиназа ( PGK); ES - пируваткиназа ( PVK); Ее - обобщенная АТРаза; Ij - фруктозо-б-фосфат ( F6P); 12 - смесь глицеральдегид-фосфата ( GAP), дигидроксиацетонфосфата ( DHAP) и фруктозе - 1 6-дифосфата ( FDP); 13 - 1 3-дифосфоглице-рат ( 1 3 - DPG); I4 - смесь фосфоенолпирувата ( PEP), 2-фосфоглицерата ( 2 - PG); и 3-фосфоглицерата ( 3 - PG); АЗ и АЗ - ADP и АТР соответственно. [9]
 |
Метаболизм фруктозы. [10] |
Образовавшийся D-глицеральдегид под влиянием соответствующей киназы ( триокиназы) подвергается фосфорилированию до глицеральде-гид-3 - фосфата. В этот же промежуточный продукт гликолиза переходит и дигидроксиацетонфосфат. [11]
Если число частиц в реакции возрастает, то уменьшение абсолютных значений концентраций компонентов будет способствовать смещению равновесия в сторону продуктов реакции. Например, реакция превращения фруктозо-1 6-дифосфата в смесь глицеральдегиД - 3-фосфата и дигидроксиацетонфосфата характеризуется довольно высоким положительным значением величины AG0 23 8 кДж / моль. [12]
Напишите последовательные этапы и суммарное уравнение для биосинтеза фосфатидилхолина по спасательному пути из олеиновой и пальмитиновой кислот, дигидроксиацетонфосфата и холина. [13]
Эта технология основана на том, что ацетальдегид связывается и поэтому не может служить акцептором водорода. Вместо ацетальдегида роль такого акцептора принимает на себя дигидроксиацетонфосфат; он восстанавливается до глицерол-3 - фос-фата и дефосфорилируется с образованием глицерола. [14]
Применение в качестве субстратов изотопно-меченных карбо-кислот является удобным инструментом исследования стереохимии ферментативного переноса протона. В отличие от органических реакций в ферментативных реакциях стереоспецифический перенос протона является скорее правилом, чем исключением, что обусловлено асимметричной природой поверхности белковой молекулы. В качестве примера можно привести две реакции изотопного обмена между дигидроксиацетонфосфатом и тритиро-ванной водой, катализируемые ферментами альдолазой и трио-зофосфатизомеразой. [15]
Страницы: 1 2