Алюмината
Cтраница 1
Алюминаты различаются содержанием кобальта и алюминия, соотношение которых в расчете на окислы может быть от 1: 10 до 1: 1; в зависимости от этого цвет алюмината - от синего до черного; так, мртаалгомпнат Со ( АЮ. [1]
Алюминаты - соединения, отвечающие составу тМхОу лА1203, где М - металл в степени окисления 1, 2 или 3, а также гидроксо - и оксоалюминаты, в которых гидроксо - и оксогруппы связаны с атомами AI, образуя анионный комплекс. [2]
Алюминаты и алюмоферриты кальция способны растворить до 5 % RO без значительного химического распада. [3]
Алюминаты и алюмоферриты кальция при гидратации образуют гидроалюминаты и гидроалюмоферриты кальция. [4]
 |
Диаграмма состояния системы СаО - А12О3. [5] |
Алюминаты ЗСаО А12О3 и 5СаО - ЗА1203 входят в состав клинкера портландцемента; 5СаО - ЗА120зг СаО - А12О3 и СаО - 2А1203 присутствуют в глиноземистом цементе, алюминат СаО - 6А1 03 - в плавленом техническом корунде. [6]
Алюминаты ЗСаО А12О3 и 5СаО ЗА12О3 входят в состав клинкера портландцемента; 5СаО ЗАЬО3, СаО А12О3 и СаО 2А12О3 присутствуют в глиноземистом цементе, алюминат СаО 6А12Оз - в плавленом техническом корунде. [7]
 |
Горение термита ( справа и термитная сварка ( с л е в а. [8] |
Алюминаты получают также и при растворении металлического алюминия в щелочах. [9]
Алюминаты рассматривают как соли метаалюминиевой кислоты НА1О2, но ионы состава А1О2 реально не существуют ни в твердых алюминатах, ни в растворах. [10]
Алюминаты, как соли слабой кислоты, в водном растворе подвержены сильному гидролизу и имеют сильно щелочную реакцию. [11]
Алюминаты, рассмотренные в товарной позиции 2841, соответствуют амфотерному гид-роксиду. [12]
Алюминаты различаются содержанием кобальта и алюминия, соотношение которых в расчете на окислы может быть от 1: 10 до 1: 1; в зависимости от этого цвет алюмината-от синего до черного; так, метаалюминат Со ( АЮ2) 2 черного цвета. [13]
Алюминаты, наиболее активных одновалентных металлов в воде хорошо растворимы, но ввиду сильного гидролиза растворы их устойчивы лишь при наличии достаточного избытка щелочи. Большинство из них в воде нерастворимо. [14]
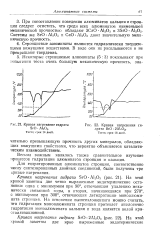 |
Кривая нагревания гидрата SrO А12О3.| Кривая нагревания гидрата SrO - 2AIoO3. [15] |
Страницы: 1 2 3 4