Дигидропроиз-водное
Cтраница 1
Дигидропроиз-водные чаще всего окисляют в хиназолины феррицианидом калия, но если алкильная группа имеет большой объем, ожидаемый продукт может и не получиться. Так, 4-грег-бутил - 3 4-дигидрохиназолии ( 190, R трет - бугил) при действии щелочного феррицианида теряет грег-бутильную групп) - и дает незамещенный хиназолин. [1]
Хотя коферменты неустойчивы по отношению к щелочи и относительно устойчивы к кислотам, дигидропроиз-водные ( легко получаемые восстановлением с помощью гипосульфита натрия) относительно устойчивы в щелочах, но совершенно неустойчивы по отношению к кислотам. При каталитическом гидрировании НАД и НАДФ получаются гексагидропроизводные, которые в отличие от дигидропроизводных не подвергаются окислению под действием флавопротеида. [2]
По Джерсдорфу [29] каждое изменение в химическом составе влечет за собой характерное изменение в токсичности независимо от других изменений. Дигидропроиз-водные, получающиеся насыщением двойных связей в боковой цепи водородом, в 1 5 раза токсичнее соответствующих ненасыщенных соединений. Ацетаты, будут ли они энольного типа или ацетилпроизводными окси-соединений, обладают токсичностью, составляющей 56 % от токсичности исходных соединений. [3]
Известны и другие производные хлортиазида и дихлортиазида, имеющие в положениях 2 -, 3 - и 6 различные заместители. Из дигидропроиз-водных хлортиазида наибольшее значение имеет циклометиазид-кристаллич. [4]
В некоторых случаях образующиеся при передаче одного электрона радикалы или ионы-радикалы малоактивны и могут накапливаться в значительных концентрациях. Такими радикалами являются семихиноны - продукты неполного восстановления хинонов в соответствующие дигидропроиз-водные. [5]
При диеновых конденсациях циклонов в качестве вторичных продуктов превращения могут образовываться и новые аддукты, возникающие в результате взаимодействия получающихся при декарбонилировании производных дигидробензола с молекулой диенофила. Если отщепление окиси углерода происходит в присутствии избытка диенофила, то дигидропроиз-водное ( VI) может вступить с ним в реакцию в качестве диена, образуя при этом новый аддукт. [6]
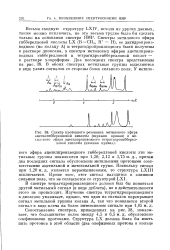 |
Спектр протонного резонанса метилового эфира ацетилгибберелловой кислоты ( верхняя кривая и метилового эфира ацетилпроизводного тетрагидрогибберелловой кислоты ( нижняя кривая. [7] |
Весьма сходную структуру LXIV, исходя из других данных, также можно исключить, но это весьма трудно было бы сделать только на основании спектра ЯМР. Спектры метилового эфира гибберелловой кислоты LX ( RCH3, R Н), ее дигидропроиз-водного ( по кольцу А) и тетрагидропроизводного были получены в растворе диоксана, а спектры метиловых эфиров ацетилпроиз-водных гибберелловой и тетрагидрогибберелловой кислот - в растворе хлороформа. В обоих спектрах метальные группы выделяются в виде узких сигналов со стороны более сильного поля. [8]
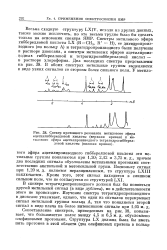 |
Спектр протонного резонанса метилового эфира ацетилгибберелловой кислоты ( верхняя кривая и метилового эфира ацетилпроизводного тетрагидрогибберелловой кислоты ( нижняя кривая. [9] |
Весьма сходную структуру LXIV, исходя из других данных, также можно исключить, но это весьма трудно было бы сделать только на основании спектра ЯМР. Спектры метилового эфира гибберелловой кислоты LX ( RCH3, R Н), ее дигидропроиз-водного ( по кольцу А) и тетрагидропроизводного были получены в растворе диоксана, а спектры метиловых эфиров ацетилпроиз-водных гибберелловой и тетрагидрогибберелловой кислот - в растворе хлороформа. В обоих спектрах метильные группы выделяются в виде узких сигналов со стороны более сильного поля. [10]
Реакция проводится в нейтральном растворителе. Если тотчас после образования соединения подвергнуть его разложению водой, спиртом или уксусной кислотой, то получается дигидропроиз-водное аценафтена. При гидролизе этого соединения большим количеством воды при 20 - 30 образуются с хорошими выходами смолистые полимерные соединения. [11]
Аналогично ведут себя также четвертичные соли гомологов 4 4 - ДП. Так, М К - диалкилтетрагидро-бис - ( 2 6-диметилпиридил) реагирует с четвертичной солью бис - ( 2 6-ди-метилпиридила) с образованием соответствующего дигидропроиз-водного. Кроме того, М Ы - диалкилтетрагидро-бис - ( 2 6-диметилпи-ридил) способен реагировать с иодалкилатами 4 4 - ДП, восстанавливая последние до Ы М - диалкилдигидро-4 4 - ДП, а сам превращаясь в четвертичную соль 2 6-диметилпиридина. N - Диметил-тетрагидродиколлидил [ из 2 4 6-триметилпиридина ( коллидина) и амальгамы натрия ] восстанавливает дииодбензилат 4 4 - ДП до йодистого тетрабензилдипиридил-виолета. На протекание реакции большое влияние оказывает природа заместителя у азота. [12]
Однако до сих пор остается спорным вопрос о том, является ли причиной активности акридиновых производных их способность замещать носители водорода в жизненно важных центрах микробной клетки. По мнению Альберта, восстановительный потенциал акридина ( - 0 3 в) слишком мал, чтобы он мог выступить в роли акцептора водорода и превратиться в малоактивное дигидропроиз-водное. С другой стороны, Брейер, Буханан и Дьюэл [77] нашли, что наиболее эффективные соединения - 5-амино -, 2, 8-диамино -, 2-аминоакридин - имеют восстановительные потенциалы - 0 916, - 0 731 и - 0 468 в, соответственно. [13]
Однако до сих пор остается спорным вопрос о том, является ли причиной активности акридиновых производных их способность замещать носители водорода в жизненно важных центрах микробной клетки. По мнению Альберта, восстановительный потенциал акридина ( - 0 3 б) слишком мал, чтобы он мог выступить в роли акцептора водорода и превратиться в малоактивное дигидропроиз-водное. С другой стороны, Брейер, Буханан и Дьюэл [77] нашли, что наиболее эффективные соединения - 5-амино -, 2, 8-диамино -, 2-аминоакридин - имеют восстановительные потенциалы - 0 916, - 0 731 и - 0 468 в, соответственно. [14]
Одновременно с ростом числа колец повышается реакционная способность соединений, особенно склонность к реакциям присоединения. Высшие члены этого ряда еще легче присоединяют указанные реагенты. Стабильность образующихся при этом дигидропроиз-водных растет с увеличением числа колец, так же как растет и стабильность соответствующих хинонов. [15]
Страницы: 1 2